题目内容
下列有关的叙述正确的是
| A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为 c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.用pH=3和pH=2的醋酸溶液中和含等量NaOH的溶液所消耗的醋酸溶液的体积分别为Va和Vb,则Va>10Vb |
| D.Na2BeO2溶液的pH>7,BeCl2溶液的pH<7,分别将它们蒸干并灼烧后,都可能生成BeO |
C
正确答案:C
A.不正确,常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序应为
c(Cl-)=c(NH4+)>c(H+)=c(OH-)
B.不正确,将pH=4的醋酸溶液稀释后,溶液中不是所有离子的浓度均降低,OH―离子浓度升高;
C.正确,弱酸越稀,电离程度越大,用pH=3和pH=2的醋酸溶液中和含等量NaOH的溶液所消耗的醋酸溶液的体积分别为Va和Vb,则Va>10Vb
D.不正确,只有BeCl2溶液蒸干并灼烧后,生成BeO

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
 、
、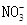 、
、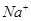 、
、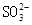
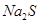 溶液中
溶液中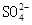 、
、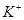 、
、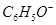 、
、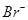
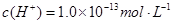 溶液中
溶液中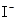 、
、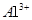
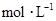 的
的 溶液中离子浓度大小排序 ________________;
溶液中离子浓度大小排序 ________________;