题目内容
(15分)A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示。请针对以下三种不同情况回答:
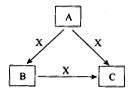
(1)若A、B、C中均含同一种常见非金属元素,将A、C的水
溶液混合可得B的沉淀
①A、B、C中含有的同一种常见非金属元素为___________。
②写出A、C的水溶液混合生成沉淀B的化学反应方程式
为 。
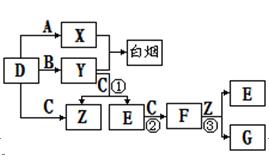
(2)若A为固态非金属单质,A与X同为第三周期元素,常温常压下C为白色固体,B分子中各原子最外层均为8e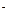 结构。
结构。
①B的电子式为_____________。
②C与水剧烈反应,生成两种常见酸,反应的化学方程式为_____________ 。
。
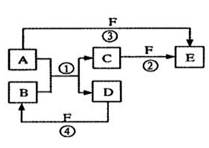
(3)若A、B、C的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。
①A中所含有的化学键是_____________。
②将过量X通入100mL 3 mol/L A的水溶液中,将所得溶液与明矾溶液混合,写出混合时反应的离子方程式___________。
③自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为__________ g。

(1)若A、B、C中均含同一种常见非金属元素,将A、C的水
溶液混合可得B的沉淀
①A、B、C中含有的同一种常见非金属元素为___________。
②写出A、C的水溶液混合生成沉淀B的化学反应方程式
为 。
(2)若A为固态非金属单质,A与X同为第三周期元素,常温常压下C为白色固体,B分子中各原子最外层均为8e
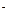 结构。
结构。①B的电子式为_____________。
②C与水剧烈反应,生成两种常见酸,反应的化学方程式为_____________
 。
。(3)若A、B、C的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。
①A中所含有的化学键是_____________。
②将过量X通入100mL 3 mol/L A的水溶液中,将所得溶液与明矾溶液混合,写出混合时反应的离子方程式___________。
③自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为__________ g。
(15分、每空2分)
(1)①硫 ②2H2S+SO2=3S↓+2H2O
(2)①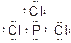 ②PCl5+4H2O=H3PO4+5HC1。
②PCl5+4H2O=H3PO4+5HC1。
(3)①离子键 共价键
② 3HCO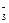 +Al3+=Al(OH)3↓+3CO2↑;
+Al3+=Al(OH)3↓+3CO2↑;
③2.65 g (3分)
(1)①硫 ②2H2S+SO2=3S↓+2H2O
(2)①
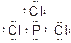 ②PCl5+4H2O=H3PO4+5HC1。
②PCl5+4H2O=H3PO4+5HC1。(3)①离子键 共价键
② 3HCO
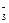 +Al3+=Al(OH)3↓+3CO2↑;
+Al3+=Al(OH)3↓+3CO2↑;③2.65 g (3分)
略

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
 (化学方程式)
(化学方程式) 
 。
。