题目内容
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g) 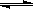 2SO3(g) △H=-190 kJ·mo1-1
2SO3(g) △H=-190 kJ·mo1-1
(1)在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=______mol·L-1·min-1
(2)下列条件的改变能加快其反应速率的是 (选填序号)
①升高温度
②保持体积不变,只增加氧气的质量
③保持体积不变,充入Ne使体系压强增大
④保持压强不变,充入Ne使容器的体积增大
(3)下列描述中能说明上述(1)反应已达平衡的是 (选填序号)
①v(O2)正=2v(SO3)逆
②SO2、O2、SO3的浓度之比为2:1:2
③单位时间内生成2n molSO2的同时生成2n mol SO3
④容器中气体的平均分子量不随时间而变化
⑤容器中气体的密度不随时间而变化
⑥容器中气体压强不随时间而变化
(4)在相同条件下发生上述反应,若要得到380kJ热量,则加入各物质的物质的量可能
是 。
| A.4 mo1SO2和2mol O2 | B.6mol SO2和6mo1 O2 |
| C.4mol SO2和4 mo1 O2 | D.6mo1 SO2和4 mo1 O2 |
(1)0.036 (2)①② (3)③④⑥ (4)BD
解析试题分析:(1)三氧化硫的反应速率为0.18mol/5L/0.5min=0.072 mol·L-1·min-1,所以v(O2)="1/2" v(SO3)= 0.036 mol·L-1·min-1
(2)①升高温度可以加快反应速率,正确;②保持体积不变,只增加氧气的质量,增大反应物的浓度,反应速率加快,正确;③保持体积不变,充入Ne使体系压强增大,体系中各物质的浓度不变,所以反应速率不变,错误;④保持压强不变,充入Ne使容器的体积增大,各物质的浓度减小,反应速率减慢,错误,答案选①②;
(3)①三氧化硫的反应速率是氧气的二倍,错误;②各物质的浓度比符合化学计量数之比时未必是平衡状态,错误;③单位时间内生成2n molSO2是逆反应速率,同时生成2n mol SO3是正反应速率,且符合化学计量数之比,正确;④气体的质量不变,而气体的物质的量一直变化,所以气体的平均相对分子质量一直变化,达平衡时保持不变,正确;⑤气体质量不变,容器体积不变,所以气体密度一直不变,错误;⑥压强在反应的过程中一直变化,达平衡时不再变化,正确,所以答案选③④⑥;
(4)A、该反应是可逆反应,反应物不可能用完,所以放出的热量小于380kJ,错误;B、6mol SO2和6mo1 O2完全反应会放出570kJ的热量,所以要得到380kJ热量是有可能的,正确;C、充入4mol SO2和4 mo1 O2时,尽管氧气的物质的量增加,但是二氧化硫的物质的量是4mol,所以二氧化硫完全反应才能得到380kJ的热量,不可能,错误;D、6mol SO2和4mo1 O2完全反应会放出570kJ的热量,所以要得到380kJ热量是有可能的,正确,答案选BD。
考点:考查反应速率的计算,条件对反应速率的影响,化学平衡的判断,对可逆反应的理解

Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式: ,该反应是 反应(填放热或吸热)。
(2)实验结果表明,催化剂的催化效果与 有关。
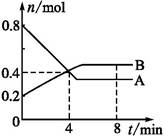
Ⅱ.某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如右图所示,图中数据分析:
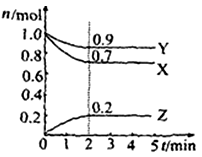
(1)该反应的化学方程式为: 。
(2)反应开始至2min,用Z表示的平均反应速率为: 。
(3)在密闭容器里,通入a mol X(g)和b mol Y(g),发生反应X(g) + Y(g) = 2Z(g),当改变下列条件时,反应速率会减小
A.降低温度 B.加入催化剂 C.增大容器体积
已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= , △H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,若反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则6s时 c(A)= mol·L-1, C的物质的量= mol;
若经一段时间后,反应达到平衡,则此时A的转化率= ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率 ( 填“变大”或“变小”或“不变”);
(3)判断该反应达到平衡的依据为 (填正确选项前的字母):
A.压强不随时间改变
B.气体的密度不随时间改变
C.c(A)不随时间改变
D.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g)
 A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。 在2 L密闭容器内,800℃时反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=__________。已知K300℃>K350℃,则该反应是________热反应。
(2)如图中表示NO2变化曲线的是__________,用O2表示从0 s~2 s 内该反应的平均速率v=________。
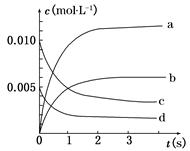
(3)能说明该反应已达到平衡状态的是__________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效催化剂
 H2+I2
H2+I2

 CH3OH(g)。工业上依此用CO生产燃料甲醇。
CH3OH(g)。工业上依此用CO生产燃料甲醇。

 增大的有____________。
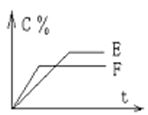
增大的有____________。 pC(气) + qD(气)的 C %与时间 t有如图关系
pC(气) + qD(气)的 C %与时间 t有如图关系