题目内容
【题目】ClO2是一种强氧化性气体(高浓度时呈红黄色,低浓度时呈黄色),在消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过下图所示装置(夹持装置略)对其进行制备、收集、吸收并制取NaClO2。
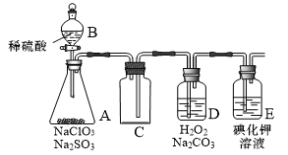
(1)仪器A的名称是______。
(2)图中装置有一明显错误,请指出:______。
(3)打开B的活塞,A中有ClO2生成,D中吸收ClO2后生成NaClO2和NaHCO3,写出D中所发生反应的离子方程式:______。
(4)E中溶液出现黄色能否说明ClO2未被H2O2和Na2CO3的混合溶液充分吸收,判断并说明理由:______。
(5)写出一种提高ClO2吸收率的方法:______。
(6)E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO2—,当pH≤2.0时,ClO2—能被I—还原。请补充完整检验E装置溶液中存在少量ClO2—的实验方案:取一定体积E装置中的溶液于分液漏斗中,______,则溶液中存在ClO2—。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
【答案】锥形瓶C装置中导气管应该长进短出2ClO2 +H2O2 +2CO32—=2ClO2—+O2↑+2HCO3—不能,因为 D 装置中有氧气产生,氧气也可能将 I 氧化为 I 2减缓稀硫酸的滴加速率(或 D 中长导管口加装多孔球泡等,合理即可)用 CCl 4 多次萃取、分液,直至溶液中滴加淀粉溶液不显蓝色。向溶液中滴加稀硫酸至溶液的 pH≤2,滴加淀粉溶液,溶液变蓝
【解析】
(1)根据仪器特征可知,仪器D的名称为锥形瓶,
因此,本题正确答案为:锥形瓶;
(2)C为ClO2气体收集装置,ClO2气体密度比空气大,C装置中导气管应该长进短出,
因此,本题正确答案为:C装置中导气管应该长进短出;
(3)D中溶液含有H2O2和Na2CO3吸收ClO2后生成NaClO2和NaHCO3,则发生氧化还原反应,ClO2作氧化剂将H2O2氧化为O2,所发生反应的离子方程式:2ClO2 +H2O2 +2CO32—=2ClO2—+O2↑+2HCO3—,
因此,本题正确答案为:2ClO2 +H2O2 +2CO32—=2ClO2—+O2↑+2HCO3—;
(4)E中溶液出现黄色可能生成了I2,由于D中生成了O2,也可能将 I 氧化为 I 2,所以不能说明ClO2未被H2O2和Na2CO3的混合溶液充分吸收,
因此,本题正确答案为:不能,因为 D 装置中有氧气产生,氧气也可能将 I 氧化为 I 2;
(5)要提高ClO2吸收率可以增加吸收时间或增大接触面积,故可采用减缓稀硫酸的滴加速率(或 D 中长导管口加装多孔球泡等),
因此,本题正确答案为:减缓稀硫酸的滴加速率(或 D 中长导管口加装多孔球泡等);
(6)根据题给信息及所提供的试剂,E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO2-,同时生成I 2,用CCl4通过多次萃取可分离出I 2,加稀硫酸调溶液pH≤2.0时,ClO2—能被I-还原生成I 2,通过淀粉溶液检验生成的I 2,即可证明溶液中存在少量ClO2—,
因此,本题正确答案为:用 CCl 4 多次萃取、分液,直至溶液中滴加淀粉溶液不显蓝色。向溶液中滴加稀硫酸至溶液的 pH≤2,滴加淀粉溶液,溶液变蓝。

 名校课堂系列答案
名校课堂系列答案