题目内容
13.下列说法正确的是( )| A. | ⅠA族元素的金属性比ⅡA族元素的金属性强 | |
| B. | ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 | |
| C. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | 短周期中次外层电子数是最外层电子数2倍的元素一定是非金属元素 |
分析 A.Ca的金属性比Na的强;
B.非金属性越强,气态氢化物越稳定,由于O易形成氢键,沸点高;
C.非金属性越强,最高价氧化物对应的水化物的酸性越强;
D.短周期中次外层电子数是最外层电子数2倍的元素,可能为Li或Si.
解答 解:A.Ca的金属性比Na的强,应为同周期ⅠA族元素的金属性比ⅡA族元素的金属性强,故A错误;
B.VIA族元素中O的非金属性最强,氢化物中稳定性最好的是H2O,由于O易形成氢键,故水的沸点高,故B正确;
C.非金属性越强,最高价氧化物对应的水化物的酸性越强,则同周期非金属最高价氧化物对应的水化物的酸性从左到右依次增强,而HClO、亚硫酸等为弱酸,但不是最高价含氧酸,故C错误;
D.短周期中次外层电子数是最外层电子数2倍的元素,可能为Li或Si,则可能为金属元素或非金属元素,故D错误,故选B.
点评 本题考查元素的性质,为高频考点,把握元素的位置及性质变化规律为解答的关键,把握元素金属性、非金属性比较即可解答,题目难度不大.

练习册系列答案
相关题目
1.下列物质中,不能与小苏打反应的是( )?
| A. | 甲酸 | B. | 乙酸 | C. | 硫酸 | D. | 乙醇 |
8.x、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知( )
| A. | x的原子序数大于y的原子序数 | |
| B. | x的电负性小于y的电负性 | |
| C. | x的离子半径大于y的离子半径 | |
| D. | x的第一电离能小于y 的第一电离能 |
5.如下性质的递变中,不正确的是( )
| A. | HCl、H2S、PH3的稳定性依次减弱 | |
| B. | HClO4、H2SO4、H3PO4的酸性依次减弱(相同条件下) | |
| C. | CsOH、KOH、LiOH的碱性依次增强 | |
| D. | Na+、Mg2+、Al3+的离子半径逐渐减小 |
2.下列图象分别表示有关反应的反应过程与能量变化的关系( )

据此判断下列说法中正确的是( )

据此判断下列说法中正确的是( )
| A. | 石墨转变为金刚石是吸热反应 | |
| B. | 相同条件下,等质量S(g)和S(s)的能量比较,S(s)能量较高 | |
| C. | 白磷比红磷稳定 | |
| D. | CO(g)+H2O(g)═CO2(g)+H2(g)是吸热反应 |


 .
. 按1:1恰好反应生成两种酸性有机物,则另一种有机物的名称为乙酸.
按1:1恰好反应生成两种酸性有机物,则另一种有机物的名称为乙酸. .试剂c最好选用C(填字母序号).
.试剂c最好选用C(填字母序号). .
. 和一个
和一个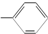 ,则该有机物可能的结构有(不考虑立体异构)( )
,则该有机物可能的结构有(不考虑立体异构)( ) 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.