题目内容
下列对实验现象的描述中错误的是
| A.向FeCl3和KSCN混合溶液中加入少量KCl固体,溶液血红色变浅 |
| B.向5mL 0.1mol/L K2Cr2O7溶液中加入少量NaOH固体,溶液由橙色变为黄色 |
| C.等体积等浓度Na2S2O3和H2SO4混合,温度升高出现浑浊和生成气体速度加快 |
| D.酸性KMnO4溶液中滴加H2C2O4,H2C2O4浓度越大褪色和生成气体速度越快 |
A
解析试题分析:A、加入少量KCl固体,溶液中Fe3+、SCN-浓度不变,K+和Cl-不参加反应,平衡不移动,溶液颜色无明显变化,故A错误;B、Cr2O72-+H2O 2CrO42-+2H+加入少量NaOH固体,中和氢离子,氢离子浓度降低,平衡向右移动,溶液由橙色变为黄色,故B正确;C、温度越高、浓度越大,则反应速率就越快,Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O,故C正确;D、该反应是一条自催化反应,即反应生成的锰离子可以作为催化剂。所以开始加入草酸溶液时,随着草酸的不断滴入,锰离子浓度增大,反应速率增大,即褪色和生成气体速度越快,故D正确。
2CrO42-+2H+加入少量NaOH固体,中和氢离子,氢离子浓度降低,平衡向右移动,溶液由橙色变为黄色,故B正确;C、温度越高、浓度越大,则反应速率就越快,Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O,故C正确;D、该反应是一条自催化反应,即反应生成的锰离子可以作为催化剂。所以开始加入草酸溶液时,随着草酸的不断滴入,锰离子浓度增大,反应速率增大,即褪色和生成气体速度越快,故D正确。
考点:化学平衡的影响因素

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列事实不能用平衡移动原理解释的是
 |      |  |  |
| A | B | C | D |
一定条件下进行反应:COCl2(g) Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入
Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入
1.0 mol COCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法正确的是
A.保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol·L-1,则反应的ΔH<0
B.若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变
C.保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.60 molCl2和0.60 molCO,反应达到平衡前的速率:v(正)<v(逆)
D.保持其他条件不变,起始向容器中充入1.0 molCl2和0.8 molCO,达到平衡时,Cl2的转化率小于60%
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(气)+xB(气) 2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
| A.平衡时,物质的量比A∶B∶C=2∶11∶4 |
| B.x值等于4 |
| C.B的平均反应速率为0.04 mol·L-1·min-1 |
| D.A的转化率20% |
在容积可变的密闭容器中存在如下反应:2A(g)+B(g) 3C(g) ΔH<0,某研究小组研究了其他条件不变时,只改变某一条件对上述反应的影响,下列分析正确的是( )
3C(g) ΔH<0,某研究小组研究了其他条件不变时,只改变某一条件对上述反应的影响,下列分析正确的是( )
| A.图Ⅰ表示的是t1时刻升高温度对反应速率的影响 |
| B.图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响 |
| C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高 |
| D.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高 |
一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
| A.缩小体积 | B.恒容,充入He | C.恒容,充入O2 | D.恒压,充入N2 |
下列事实,不能用勒夏特列原理解释的是
| A.硫酸工业中,增大O2的浓度有利于提高SO2的转化率 |
B.对2HI H2+I2平衡体系增加压强使颜色变深 H2+I2平衡体系增加压强使颜色变深 |
| C.开启啤酒瓶后,瓶中立刻泛起大量泡沫 |
| D.滴有酚酞的氨水溶液,适当加热溶液(氨气不挥发)后颜色变深 |
下列有关说法正确的是 ( )
| A.合成氨反应需使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动 |
| B.常温下,将pH =10的氨水稀释,溶液中所有离子浓度都减小 |
| C.100 mL pH=3的HA和HB分别与足量的锌反应,HA放出的氢气多,说明HA酸性比HB弱 |
D.已知  I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
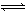 2C来说,以下表示的化学反应速率最快的是
2C来说,以下表示的化学反应速率最快的是