题目内容
依据事实,写出下列反应的热化学方程式。
(1)在25℃、101 kPa下,1 g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为 ______________________。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为_______________________________________________。
(1)在25℃、101 kPa下,1 g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为 ______________________。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为_______________________________________________。
(1)CH3OH(l)+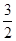 O2(g)===CO2(g)+2H2O(l) ΔH=-725.76 kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH=-725.76 kJ·mol-1
(2)N2(g)+2O2(g)===2NO2(g) ΔH=+67.8 kJ·mol-1
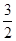 O2(g)===CO2(g)+2H2O(l) ΔH=-725.76 kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH=-725.76 kJ·mol-1(2)N2(g)+2O2(g)===2NO2(g) ΔH=+67.8 kJ·mol-1
试题分析:(1)燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以1mol甲醇完全燃烧放出的热量是22.68 kJ×32=725.76 kJ,则示甲醇燃烧热的热化学方程式为CH3OH(l)+
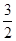 O2(g)===CO2(g)+2H2O(l) ΔH=-725.76 kJ·mol-1。
O2(g)===CO2(g)+2H2O(l) ΔH=-725.76 kJ·mol-1。(2),每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为N2(g)+2O2(g)===2NO2(g) ΔH=+67.8 kJ·mol-1。
点评:该题是基础性试题的考查,侧重对学生基础知识的训练。该题的关键是明确热化学方程式的含义以及书写注意事项,有利于培养学生规范的答题能力,提高学生的应试能力和学习效率。

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目

 CH3COOK+H2O
CH3COOK+H2O
 2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图⑶所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。则:
2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图⑶所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。则: 的绝对值均正确)( )
的绝对值均正确)( ) (燃烧热)
(燃烧热) (中和热)
(中和热) =-269kJ/mol (反应热)
=-269kJ/mol (反应热)