题目内容
已知X、Y为有刺激性气味的气体,有如图转化关系,部分产物未标出.
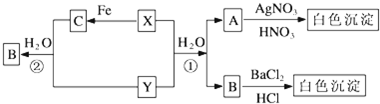
试回答:
(1)写出下列物质的化学式
X 、Y 、A .
(2)反应①的化学方程式为 ,反应②的离子方程式为 .

试回答:
(1)写出下列物质的化学式
X
(2)反应①的化学方程式为
考点:无机物的推断
专题:推断题
分析:A与硝酸银溶液、稀硝酸生成白色沉淀可知A中含有Cl-;B与氯化钡溶液、盐酸生成白色沉淀可知B中含有SO42-;X、Y、H2O生成Cl-和SO42-且X、Y均是有刺激性气味的气体可推知X、Y是二氧化硫和氯气,反应为SO2+Cl2+2H2O=H2SO4+2HCl;X能与铁反应可知X为Cl2,则C为FeCl3、Y为SO2,二氧化硫通入氯化铁溶液生成氯化亚铁、硫酸和盐酸,则A为HCl,B为H2SO4,结合对应物质的性质以及题目要求解答该题.
解答:
解:A与硝酸银溶液、稀硝酸生成白色沉淀可知A中含有Cl-;B与氯化钡溶液、盐酸生成白色沉淀可知B中含有SO42-;X、Y、H2O生成Cl-和SO42-且X、Y均是有刺激性气味的气体可推知X、Y是二氧化硫和氯气,反应为SO2+Cl2+2H2O=H2SO4+2HCl;X能与铁反应可知X为Cl2,则C为FeCl3、Y为SO2,二氧化硫通入氯化铁溶液生成氯化亚铁、硫酸和盐酸,则A为HCl,B为H2SO4,
(1)由以上分析可知X为Cl2,Y为SO2,A为HCl,故答案为:Cl2;SO2;HCl;
(2)X、Y是二氧化硫和氯气,反应①为SO2+Cl2+2H2O=H2SO4+2HCl,二氧化硫通入氯化铁溶液生成氯化亚铁、硫酸和盐酸,反应②的离子方程式为反应的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+,
故答案为:Cl2+SO2+2H2O═2HCl+H2SO4;2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.
(1)由以上分析可知X为Cl2,Y为SO2,A为HCl,故答案为:Cl2;SO2;HCl;
(2)X、Y是二氧化硫和氯气,反应①为SO2+Cl2+2H2O=H2SO4+2HCl,二氧化硫通入氯化铁溶液生成氯化亚铁、硫酸和盐酸,反应②的离子方程式为反应的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+,
故答案为:Cl2+SO2+2H2O═2HCl+H2SO4;2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.
点评:本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合运用的考查,注意本题推出A中含有Cl-、B中含有SO42-后逆推X、Y要联想X、Y应是含有Cl和S的有刺激性气味的气体,常见的为Cl2和SO2,题目难度中等.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
下列反应的离子方程式书写正确的是( )
A、用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-
| ||
| B、用二氧化硫水溶液吸收溴蒸气:SO2+Br2+2H2O=2H++SO42-+2HBr | ||
| C、在(NH4)2SO4溶液中逐滴加入少量的Ba(OH)2溶液:NH4++SO42-+Ba2++OH-=BaSO4↓+NH3?H2O | ||
| D、次氯酸钙溶液中通入少量SO2气体:Ba2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
NA为阿伏加德罗常数,下列叙述错误的是( )
| A、0.1mol Na2O2与足量水完全反应时,转移电子数目为0.1NA |
| B、12g金刚石含有的共价键数为2NA |
| C、0.1mol的铜与足量的浓硫酸反应生成SO2的体积(标况)约为2.24L |
| D、在1L 0.1mol?L-1碳酸钠溶液中阴离子总数小于0.1NA |

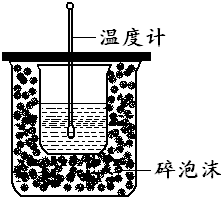 在如图所示的装置中进行中和反应的反应热测定,实验操作如下:
在如图所示的装置中进行中和反应的反应热测定,实验操作如下: