题目内容
【题目】某气态烃在标准状况下的密度为3.215g/L,现取3.6g该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4g,碱石灰增重11g,求:
(1)该烃分子的摩尔质量.
(2)确定该烃的分子式.
(3)已知该烃的一氯代物只有一种,写出该烃的结构简式.
【答案】
(1)解:烃的摩尔质量为3.215g/L×22.4L/mol=72g/mol,
答:该烃的摩尔质量为72g/mol;
(2)解:生成水的物质的量为n(H2O)= ![]() =0.3mol,所以n(H)=2n(H2O)=0.3mol×2=0.6mol
=0.3mol,所以n(H)=2n(H2O)=0.3mol×2=0.6mol
生成CO2的物质的量为n(CO2)= ![]() =0.25mol,所以n(C)=n(CO2)=0.25mol
=0.25mol,所以n(C)=n(CO2)=0.25mol
烃中C原子、H原子的个数比为0.25mol:0.6mol=5:12,实验式为C5H12,最简式相对分子质量为72,实验式即是分子式,所以该烃的分子式为C5H12.
答:该烃的分子式为C5H12;
(3)解:C5H12是烷烃,该烃的一氯代物只有一种,分子中只有一种H原子,故该烃结构简式为 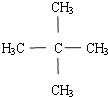 .
.
答:烃的结构简式  .
.
【解析】(1)摩尔质量=密度×气体摩尔体积;(2)浓硫酸增重5.4g为生成的水的质量,碱石灰增重11g为燃烧生成CO2的质量,根据C原子、H原子守恒可计算出3.6g烃中C原子、H原子的个数比,即求出的实验式,再结合烃的相对分子质量确定其分子式.(3)一氯代物只有一种,则分子中只有一种H原子,据此解答.

练习册系列答案
相关题目


