题目内容
【题目】[物质结构与性质]
[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN

(1)Zn2+基态核外电子排布式为____________________。
(2)1 mol HCHO分子中含有σ键的数目为____________mol。
(3)HOCH2CN分子中碳原子轨道的杂化类型是______________。
(4)与H2O分子互为等电子体的阴离子为________________。
(5)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为_____________。
【答案】(1)1s22s22p62s23p63d10(或[Ar] 3d10)(2)3;(3)sp3和sp;(4)NH2-;
(5) ;
;
【解析】
试题分析:(1)Zn是30号元素,Zn2+核外有28个电子,根据原子核外电子排布规律可知基态Zn2+核外电子排布式为1s22s22p62s23p63d10;
(2)甲醛的结构式是![]() ,由于单键都是σ键,双键中有一个σ键和一个π键,因此在一个甲醛分子中含有3个σ键和1个π键,所以在1 mol HCHO分子中含有σ键的数目为3 mol;
,由于单键都是σ键,双键中有一个σ键和一个π键,因此在一个甲醛分子中含有3个σ键和1个π键,所以在1 mol HCHO分子中含有σ键的数目为3 mol;
(3)根据HOCH2CN的结构简式可知在HOCH2CN分子中,连有羟基-OH的碳原子形成4个单键,因此杂化类型是sp3杂化,含有—CN的碳原子与N原子形成三键,则取轨道的杂化轨道类型是sp杂化;
(4)原子数和价电子数分别都相等的是等电子体,H2O含有10个电子,则与H2O分子互为等电子体的阴离子为NH2-;
(5)在[Zn(CN)4]2-中Zn2+与CN-的N原子形成配位键,N原子提供一对孤对电子,Zn2+的空轨道接受电子对,因此若不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为 。
。

【题目】硫代硫酸钠晶体(Na2S2O3·5H2O,式量248) 可用于照相行业的定影剂。它易溶于水,且溶解度随温度升高而显著增大,难溶于乙醇,加热时易分解,实验室模拟工业制备硫代硫酸钠晶体通常有两种方法。(硫单质不溶于水,微溶于酒精)
I 亚硫酸钠法:Na2SO3+S+5H2O=Na2S2O3·5H2O,简易实验流程如下:

(1)硫粉用乙醇润湿的目的是 ;
(2)洗涤粗产品,下列洗涤剂最合适的是 ;
A.冰水 B.热水 C.乙醇 D.乙醇-水混合溶液
(3)所得粗产品一般通过 方法提纯;
II硫化碱法:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,主要实验装置如下:
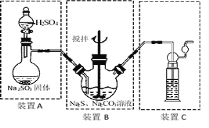
(4)装置C中可放入 ;
A.BaCl2溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.NaOH溶液
(5)为测定粗产品中Na2S2O35H2O的纯度。某兴趣小组称取5.0 g粗产品配成250mL溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL 0.01mol/L KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时到达滴定终点。实验数据如下表:
滴定次数 | 1 | 2 | 3 |
消耗Na2S2O3溶液(mL) | 19.98 | 21.18 | 20.02 |
该产品的纯度是 ;
(6)硫代硫酸钠产率受温度、pH影响如下图:

下列说法不正确的是 。
A.生成Na2S2O3一定是放热反应
B. 制备应采取较低温度
C.Na2S2O3一定能和0.1mol·L-1的硫酸发生反应
D.控制pH和温度,可以提高Na2S2O3的产率


