题目内容
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性。常温下,0.1molL﹣1 t溶液与0.1molL﹣1 u溶液的pH 均为1。下列说法不正确的是( )

A. Y、W的最高价氧化物对应的水化物均为强酸
B. 原子半径:X<Z<Y
C. s溶于水的反应中,氧化剂与还原剂的物质的量之比为1:2
D. v的电子式可表示为![]()
【答案】D
【解析】短周期主族元素X、Y、Z、W的原子序数依次增大。由图中物质转化关系及p和s均为有色气体,v的水溶液呈碱性,常温下,0.1molL-1 t溶液与0.1molL-1 u溶液的pH 均为1可知,v为NH3,p为Cl2,u为HCl,q为H2,m为N2,n为O2,r为NO,s为NO2,t为HNO3,p、s分别为黄绿色、红棕色;又p、q、m、n分别是元素W、X、Y、Z的气体单质,则X为H,Y为N,Z为O,W为Cl,A.Y、W的最高价氧化物对应的水化物分别为硝酸、高氯酸,均为强酸,A正确;B.电子层越多原子半径越大、同周期从左向右原子半径减小,则原子半径:X<Z<Y,B正确;C.s为NO2,与水反应生成硝酸和NO,NO2既是氧化剂,又是还原剂,结合元素的化合价变化可知,氧化剂与还原剂的物质的量之比为1:2,C正确;D.v为NH3,属于共价化合物,其电子式为![]() ,D错误;答案选D。
,D错误;答案选D。

 冲刺100分单元优化练考卷系列答案
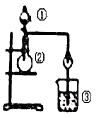
冲刺100分单元优化练考卷系列答案【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
B | 浓氨水 | 碱石灰 | Al2(SO4)3溶液 | Al(OH)3具有两性 | |
C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
D | 稀盐酸 | Na2CO3 | Na2SiO3 | 非金属性:C>Si |
A.A
B.B
C.C
D.D