题目内容
【题目】下列图示与对应的叙述相符的是![]()
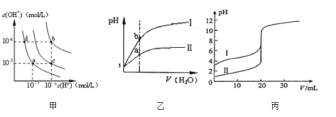
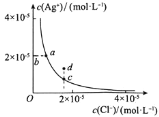
A.图甲中纯水仅升高温度,就可以从a点变到c点
B.图甲中在b点对应温度下,将pH=2的H2SO4溶液与pH=10的NaOH溶液等体积混合后,溶液显中性
C.图乙表相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
D.图丙表示25℃时用0.100molL-1NaOH溶液分别滴定20.00ml0.100molL-1的盐酸和醋酸,V(NaOH)=20.00ml时,两份溶液中c(Cl-)=c(CH3COO-)
【答案】B
【解析】
A. 纯水升高温度,H+和OH-浓度均增大;
B. b点Kw=10-12,中性溶液pH=6;
C.醋酸为弱酸,稀释促进电离,加水稀释后醋酸的pH较小;
D. V(NaOH)=20.00ml时,两种溶液中的溶质分别是CH3COONa和NaCl,醋酸根离子水解,Cl-不水解;
A. 纯水升高温度,H+和OH-浓度均增大,图中从a点变为c点,OH-浓度不变,A项错误;
B. b点Kw=10-12,中性溶液pH=6,将pH=2的H2SO4与pH=10的NaOH溶液等体积很合,c(H+)=c(OH-),等体积混合,溶液呈中性,B项正确;
C. 醋酸为弱酸,稀释促进电离,加水稀释后醋酸的pH较小,曲线II为醋酸,且b点溶液的导电性比a点弱,C项错误;
D. V(NaOH)=20.00ml时,两种溶液中的溶质分别是CH3COONa和NaCl,醋酸根离子水解,Cl-不水解,因此c(Cl-)>c(CH3COO-),D项错误;
答案选B。

 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案【题目】某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。查阅资料:
平衡Ⅰ:![]()
平衡Ⅱ:![]()
项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+/mgL-1 | 72 | ≤0.5 |
NH4+/mgL-1 | 2632 | ≤15 |
下列说法错误的是( )
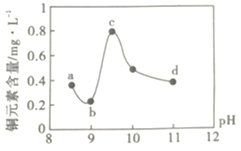
A.a~b段发生的反应为:![]()
B.b~c段:随pH升高,Cu(OH)2的量增加,导致平衡Ⅰ正向移动,铜元素含量上升
C.c~d段:随pH升高,c(OH-)增加,平衡Ⅰ逆向移动,铜元素含量下降
D.d点以后,随c(OH-)增加,铜元素含量可能上升
【题目】在2 L密闭容器内,800℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应达到平衡时,NO的物质的量浓度为__________ mol/L;升高温度,NO的浓度增大,则该反应是________(填“放热”或“吸热”)反应。
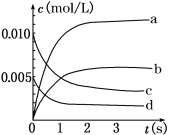
(2)如下图中表示NO2变化的曲线是________(填字母序号a、b、c、d)。用O2表示从0~2 s内该反应的平均速率v=________ mol/(L·s)。
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂