题目内容
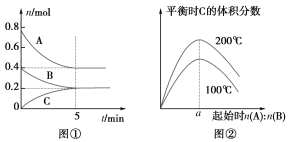
【题目】20mL0.1000mol·L-1氨水用0.1000mol·L-1的盐酸滴定,滴定曲线如图,下列说法正确的是( )
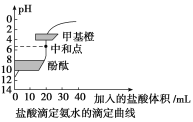
A.该中和滴定适宜用酚酞作指示剂
B.两者恰好中和时,溶液的pH=7
C.达到滴定终点时,溶液中:c(H+)=c(OH-)+c(NH3·H2O)
D.当滴入盐酸达30 mL时,溶液中c(NH4+)+c(H+)<c(OH-)+c(Cl-)
【答案】C
【解析】
A.反应终点生成氯化铵,水解显酸性,酚酞的变色范围为8~10,应选甲基橙作指示剂,故A错误;
B.两者恰好中和时生成氯化铵,溶液的pH<7,故B错误;
C.物料守恒式为c(NH4+)+c(NH3H2O)=c(Cl-),电荷守恒式为c(NH4+)+c(H+)=c(OH-)+c(Cl-),则c(H+)=c(OH-)+c(NH3H2O),故C正确;
D.溶液不显电性,遵循电荷守恒,则当滴入盐酸达30mL时,溶液中c(NH4+)+c(H+)=c(OH-)+c(Cl-),故D错误;
故答案为C。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案【题目】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Na+、K+、Cu2+ |
阴离子 | SO42-、OH- |
如图1所示装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了16 g。常温下各烧杯中溶液的pH与电解时间t的关系如图2所示。请回答下列问题:
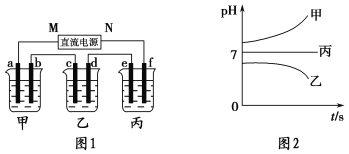
(1)M为直流电源的________极,b电极上发生的电极反应为______________________。
(2)计算e电极上生成的气体在标准状况下的体积为________________。
(3)写出乙烧杯中的总反应方程式:____________________________________________。