题目内容
【题目】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
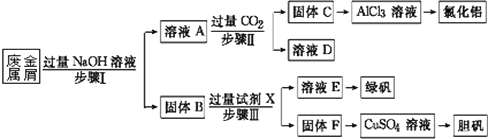
请回答:
(1)写出步骤Ⅰ中Al与NaOH溶液反应的离子方程式_________。
(2)试剂X是_______;固体F是______。
(3)在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。一段时间后,观察到烧杯中产生
的白色沉淀会逐渐减少。为避免固体C减少,可在a和b间加一个盛有饱和____溶液的洗气瓶,其作用是______。

(4)使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式________。
【答案】2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ 稀硫酸 铜 NaHCO3 除去CO2中的HCl气体 2Fe3++Fe=3Fe2+
【解析】
Fe、Cu、Fe2O3都不与NaOH溶液反应,Al和Al2O3可与NaOH溶液反应,用含有Al、Fe、Cu和Al2O3、Fe2O3的废金属屑制取AlCl3、绿矾晶体(FeSO47H2O)和胆矾晶体流程为:合金中Al、Al2O3与NaOH反应,所得滤液A为NaAlO2溶液,经途径Ⅱ与足量CO2发生反应:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,反应生成Al(OH)3固体C,生成的Al(OH)3再和盐酸反应生成AlCl3,得到的AlCl3较纯净;溶液D为NaHCO3溶液;滤渣B为Fe、Cu及Fe2O3,为了获得绿矾,根据元素守恒,加入足量稀硫酸,得到的滤液E为FeSO4,经蒸发浓缩、冷却结晶可得到绿矾,滤渣F为Cu,可用于制备胆矾,以此解答该题。
(1) 步骤Ⅰ中Al与NaOH溶液反应产生四羟基合铝酸钠和氢气,反应的离子方程式2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑;
(2)固体B是Fe、Cu、Fe2O3的混合物,向其中加入稀硫酸,金属铜和稀硫酸不反应,但是金属铁可以和稀硫酸反应生成硫酸亚铁和氢气,氧化铁与硫酸反应生成硫酸铁,硫酸铁与铁化合成硫酸亚铁,进而制得绿矾晶体,所以试剂X为稀硫酸,固体F是Cu单质;
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂将制得的CO2气体通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是二氧化碳气体中含有从盐酸中挥发出的HCl气体,氯化氢在水中溶解了部分Al(OH)3沉淀,发生的反应为Al(OH)3+3H+=Al3++3H2O,为了避免固体C减少,可在制取二氧化碳的装置与收集装置之间增加一个洗去HCl的装置,同时不溶解CO2,二氧化碳在饱和NaHCO3中难溶,氯化氢和NaHCO3反应生成二氧化碳气体,所以可在装置a和b之间增加一个盛有饱和NaHCO3溶液的洗气瓶,除去二氧化碳中的氯化氢;
故答案为:在装置a和b之间增加一个盛有饱和NaHCO3溶液的洗气瓶,除去HCl;
(4) 使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,这时Fe单质与Fe3+发生氧化还原反应产生Fe2+,该反应的离子方程式为2Fe3++Fe=3Fe2+,从而达到除杂的目的。

【题目】已知下列元素的原子半径
原子 | N | S | O | Si |
半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
根据以上数据,磷原子的半径可能是
A.0.80×10-10mB.1.10×10-10mC.1.20×10-10mD.0.70×10-10m
【题目】Ⅰ.在0.1 mol·L-1的重铬酸钾(K2Cr2O7)溶液中存在如下平衡:
Cr2O72-+H2O![]() 2HCrO4
2HCrO4![]() 2CrO42-+2H+
2CrO42-+2H+
(1)重铬酸钾溶液呈______性,在强碱溶液中,铬元素的主要存在形式为________(填离子符号),向重铬酸钾溶液中加入适量稀硫酸,溶液中c(Cr2O72-)/c(CrO42-)将______(填“增大”、“减小”或“不变”)。
Ⅱ.已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)若溶液中只溶解了一种溶质,则该溶质是 ________,上述四种离子浓度的大小顺序为________(选填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为________;
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_______c(NH3·H2O) (填“大于”“小于”或“等于”)。
III.重金属离子对河流海洋造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含有Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1。排放前拟用沉淀法除去这两种
离子,查找有关数据如下:
难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
(1)你认为往废水中投入________________(填字母序号),沉淀效果最好。
A. NaOH B.Na2S C.KI D. Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=_______。


