题目内容
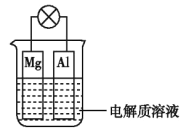
【题目】为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的工作原理如图所示。下列说法正确的是( )
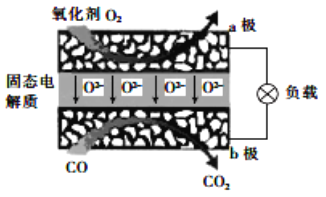
A. 正极的电极反应式为 O2+4e-+2H2O===4OH-
B. 还可以选用 NaOH 固体作固态电解质
C. 若反应中转移 1 mol 电子,则生成 22.4LCO2
D. 电子从 b 极经导线流向 a 极
【答案】D
【解析】A. 通入氧气的a电极是正极,正极上氧气得电子发生还原反应,电极反应式为O2+4e-═2O2-,故A错误;B.因为NaOH与CO2会发生反应,所以不可以选用NaOH固体作固态电解质,故B错误;C .CO所在的b电极为负极,电极反应式为![]() ,所以反应中转移1mol电子,则生成
,所以反应中转移1mol电子,则生成![]() (标准状况)CO2,故D错误;D. 外电路中,电子从负极b极经导线流向正极a极,所以A正确;答案: D。
(标准状况)CO2,故D错误;D. 外电路中,电子从负极b极经导线流向正极a极,所以A正确;答案: D。

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
【题目】I.一定量的CO(g)和H2O(g)分别通入容积为1L的恒容密闭容器中,发生反应CO(g)+H2OCO2(g)+H2(g)得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衝所需时间/min | |
CO | H2O | CO2 | |||
1 | 500 | 8 | 4 | 3.2 | 4 |
2 | 700 | 4 | 2 | 0.8 | 3 |
3 | 700 | 4 | 2 | 0.8 | 1 |
(1)①下列情况表明反应达到平衡状态的是 (填序号)
A.CO2和H2生成速率相等
B.温度不变时,压强不变
C.生成CO2的速率和生成CO的速率相等
②实验2中,反应达到平衡状态时,CO的转化率为 .
③实验3和实验2相比,改变的条件是 .
(2)①硫化钠溶液具有较强碱性,其原因是(用离子方程式表示).
②欲使0.1mol的Na2S溶液中, ![]() 的值增大,可采取的措施是(填序号)
的值增大,可采取的措施是(填序号)
A.加适量等浓度的NaOH溶液
B.加适量的水
C.通入适量的H2S气体.