题目内容
对于可逆反应N2(g)+3H2(g)?2NH3(g)△H<0.如表所示研究目的和图示相符的是( )
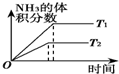
分析:A、依据先拐先平温度高分析,合成氨是放热反应,温度越高平衡逆向进行,氨气体积分数减小,温度越高速率越大,图象T2条件斜率应大;
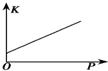
B、平衡常数随温度变化;
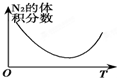
C、图象分析可知是氮气体积分数减小后再增大,说明开始反应正向进行氮气体积分数最低时,反应达到平衡,后续升温是对化学平衡的影响,反应是放热反应,升温平衡逆向进行;
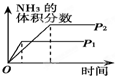
D、依据先拐先平压强大分析,反应是气体体积减小的反应,增大压强平衡正向进行,氨气体积分数增大,压强大反应速率大.先达到平衡;
B、平衡常数随温度变化;
C、图象分析可知是氮气体积分数减小后再增大,说明开始反应正向进行氮气体积分数最低时,反应达到平衡,后续升温是对化学平衡的影响,反应是放热反应,升温平衡逆向进行;
D、依据先拐先平压强大分析,反应是气体体积减小的反应,增大压强平衡正向进行,氨气体积分数增大,压强大反应速率大.先达到平衡;
解答:解:A、依据先拐先平温度高分析,合成氨是放热反应,温度越高平衡逆向进行,氨气体积分数减小,温度越高速率越大,图象T2条件斜率应大,故A错误;
B、平衡常数随温度变化,不随压强变化,故B错误;
C、图象分析可知是氮气体积分数减小后再增大,说明开始反应正向进行氮气体积分数最低时,反应达到平衡,后续升温是对化学平衡的影响,反应是放热反应,升温平衡逆向进行,氮气体积分数增大,故C正确;
D、依据先拐先平压强大分析,反应是气体体积减小的反应,增大压强平衡正向进行,氨气体积分数增大,压强大反应速率大,先达到平衡,需要的时间短,故D错误;
故选C.
B、平衡常数随温度变化,不随压强变化,故B错误;
C、图象分析可知是氮气体积分数减小后再增大,说明开始反应正向进行氮气体积分数最低时,反应达到平衡,后续升温是对化学平衡的影响,反应是放热反应,升温平衡逆向进行,氮气体积分数增大,故C正确;
D、依据先拐先平压强大分析,反应是气体体积减小的反应,增大压强平衡正向进行,氨气体积分数增大,压强大反应速率大,先达到平衡,需要的时间短,故D错误;
故选C.
点评:本题考查了化学平衡图象分析判断,化学平衡的建立和影响平衡的因素分析判断是解题关键,注意图象中表示的反应速率的改变,题目难度中等.

练习册系列答案
相关题目