题目内容
【题目】(1)某种苯的同系物0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。实践中可根据核磁共振氢谱(PMR)上观察到氢原子给出的峰值情况,确定有机物的结构。此含有苯环的有机物,在PMR谱上峰给出的稳定强度仅有四种,它们分别为:①3∶1∶1 ②1∶1∶2 ∶6 ③3∶2 ④3∶2∶2∶2∶1 ,请分别推断出其对应的结构:
①_______________________________; ②______________________________;
③_______________________________; ④______________________________。
(2)下表中括号内物质为所含的少量杂质,请选用适当的试剂和分离装置将杂质除去,并将所选的试剂及装置的编号填入表中。
试剂:①水; ②氢氧化钠; ③溴水; ④酸性高锰酸钾
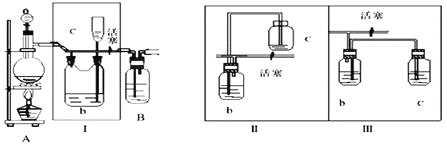
分离装置:A.分液装置; B.蒸馏装置; C.洗气装置;
需加入的试剂 | 分离装置 | |
乙烷(乙烯) | __________________ | __________________ |
乙醇(乙酸) | __________________ | __________________ |
【答案】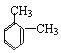
![]()
![]()
![]() ③ C ④ B
③ C ④ B
【解析】
(1)浓硫酸增重质量为水的质量,根据水的质量计算其中含有的H原子的物质的量;氢氧化钠溶液增重的质量为CO2的质量,根据CO2的质量计算其中含有的C原子的物质的量,进而可推算出1mol有机物中含有C、H的物质的量,得到其分子式,根据核磁共振氢谱可知有几种性质不同的H,且知道了原子个数比,以此可确定有机物的分子式,并书写结构简式;
(2)乙烯与溴水反应,而乙烷不能;乙酸与NaOH反应后,增大与乙醇的沸点差异,以此来解答。
(1)浓硫酸增重9g为H2O的质量,则n(H)=2×n(H2O)= 2×![]() =1mol;氢氧化钠溶液增重35.2g为CO2的质量,则n(C)=n(CO2)=
=1mol;氢氧化钠溶液增重35.2g为CO2的质量,则n(C)=n(CO2)=![]() =0.8mol,所以1mol有机物中含有8molC,10molH,则该苯的同系物的分子式为C8H10。
=0.8mol,所以1mol有机物中含有8molC,10molH,则该苯的同系物的分子式为C8H10。
①在PMR谱上峰给出的稳定强度为:3:1:1,即有三种类型的氢原子,个数之比是3:1:1,则为邻二甲苯,结构简式为: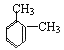 ;
;
②在PMR谱上峰给出的稳定强度为:1:1:2:6,即有4种类型的氢原子,个数之比是1:1:2:6,则为间二甲苯,结构简式为: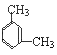 ;
;
③在PMR谱上峰给出的稳定强度为:3:2,即有2种类型的氢原子,个数之比是3:2,则为对二甲苯,结构简式为:![]() ;
;
④在PMR谱上峰给出的稳定强度为:3:2:2:2:1,即有5种类型的氢原子,个数之比是3:2:2:2:1,则为乙苯,结构简式为:![]() ;
;
(2)乙烯与溴水反应,而乙烷不能,则选择试剂为③,分离方法为洗气,即为C;
乙酸与NaOH反应后产生离子化合物CH3COONa,物质的沸点较高,而乙醇是由分子构成的化合物,沸点低,容易气化,乙醇反应后增大与乙醇的沸点差异,可选择试剂为②,分离方法为蒸馏,即为B。

 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案