题目内容
【题目】2019年8月《Green Chemistry》报道了我国学者发明的低压高效电催化还原CO2的新方法,其总反应为NaCl+CO2![]() CO+NaClO。下列有关化学用语表示错误的是( )
CO+NaClO。下列有关化学用语表示错误的是( )
A.中子数为12的钠原子:![]() NaB.Cl-的结构示意图:
NaB.Cl-的结构示意图:![]()
C.CO2的结构式:O=C=OD.NaClO的电子式:![]()
【答案】D
【解析】
A. 钠是11号元素,中子数为12的钠原子,质量数为23:![]() Na ,故A正确;
Na ,故A正确;
B. 氯的核电荷为17,最外层得到1个电子形成稳定结构,Cl-的结构示意图:![]() ,故B正确;
,故B正确;
C. 二氧化碳的碳与氧形成四个共用电子对,CO2的结构式:O=C=O,故C正确;
D. NaClO是离子化合物,NaClO的电子式: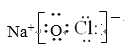 ,故D错误;
,故D错误;
故选D。

 全程金卷系列答案
全程金卷系列答案【题目】某实验小组用0.50 mol·L-1NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1NaOH溶液
(1)若实验中大约要使用470 mL NaOH溶液,至少需要称量NaOH固体____g。
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):____。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
| |
序号 | a | b | c | d | e | f |
Ⅱ.测定中和热
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、盐酸、NaOH溶液,尚缺少的实验玻璃用品是____。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ___ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol·L-1NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=______(取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母)____。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
【题目】已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
元素 | 相关信息 |
T | T元素可形成自然界硬度最大的单质 |
W | W与T同周期,核外有一个未成对电子 |
X | X原子的第一电离能至第四电离能分别是:I1=578kJ·mol-1,I2=1817kJ·mol-1,I3=2745kJ·mol-1,I4=11575kJ·mol-1 |
Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
Z | Z的一种同位素的质量数为63,中子数为34 |
(1)TY2是一种常用的溶剂,是__(填“极性分子”或“非极性分子”),分子中存在 ___个![]() 键。W的最简单氢化物容易液化,理由是___。
键。W的最简单氢化物容易液化,理由是___。
(2)在25℃、101kPa下,已知13.5g的X固体单质在O2中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为__。
(3)基态Y原子中,电子占据的最高能层符号为__;该能层具有的原子轨道数为___、电子数为___,Y、氧、W元素的电负性由大到小的顺序为___(用元素符号作答)。
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g·cm-3,则晶胞边长为___;
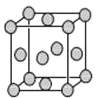
ZYO4常作电镀液,其中YO42-的空间构型是__,其中Y原子的杂化轨道类型是___,Z的单质与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2(超氧酸![]() 不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是__。
不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是__。
A.O2是氧化剂 B.HO2是氧化产物
C.HO2在碱中能稳定存在 D.1molZ参加反应有1mol电子发生转移