题目内容
下列有关化学实验图像表现的内容错误的是( )
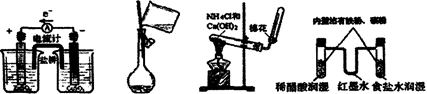

| A.铜锌原电池 | B.转移溶液 | C.氨的制取装置 | D.模拟铁锈蚀装置 |
A
A选项的正确实验图像为:

在有盐桥的原电池中,负极对应的电解质溶液阳离子与负极材料金属相同,一般正极对应的电解质溶液阳离子与正极材料金属相同。在原电池中,电子转移的方向为负极经导线流向正极。

在有盐桥的原电池中,负极对应的电解质溶液阳离子与负极材料金属相同,一般正极对应的电解质溶液阳离子与正极材料金属相同。在原电池中,电子转移的方向为负极经导线流向正极。

练习册系列答案
相关题目
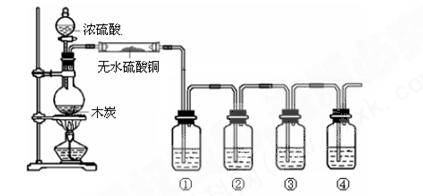
 是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。
是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。 酸 C.硝酸钾溶
酸 C.硝酸钾溶 液 D.硫化钠溶液
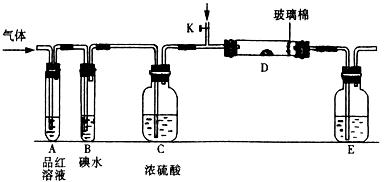
液 D.硫化钠溶液 l2与含X的溶液反应的离子方程式 。
l2与含X的溶液反应的离子方程式 。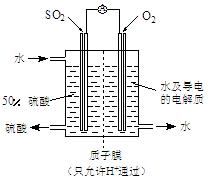

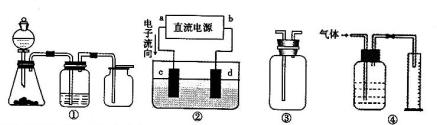
 ,a为正扳,d为阳极
,a为正扳,d为阳极 2、NH3、Cl2,、HCl、NO2等
2、NH3、Cl2,、HCl、NO2等 .装置④能用于测量气体体积
.装置④能用于测量气体体积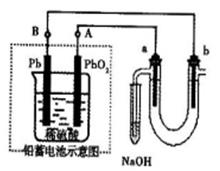
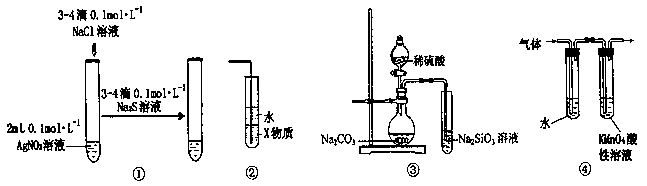
 色到 色;
色到 色; 中氨的催化氧化,回答下列问题:
中氨的催化氧化,回答下列问题: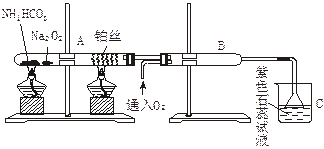
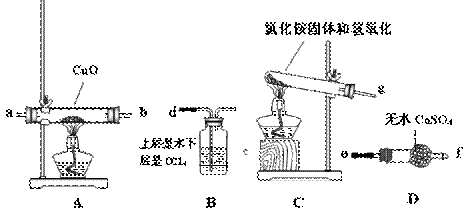 ①请你根据提供的装置从左至右连接接口序号( )()( )( )( )( )
①请你根据提供的装置从左至右连接接口序号( )()( )( )( )( )