题目内容
【题目】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A (g)+xB(g)2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如图所示.下列说法中正确是( ) 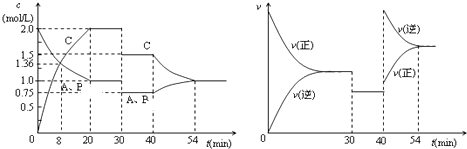
A.8min前A的平均反应速率为0.08mol/(Ls)
B.30min时扩大容器的体积,40min时升高温度
C.反应方程式中的x=1,正反应为吸热反应
D.30min和54min的反应的平衡常数相等4
【答案】B
【解析】解:A.0~8min内A的浓度减少了0.64mol/L,故v(A)= ![]() =0.08mol/(Lmin),选项中单位不对,故A错误;B.由图象可知,由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1.30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强;40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,增大压强平衡不移动,应是升高温度,故B正确;
=0.08mol/(Lmin),选项中单位不对,故A错误;B.由图象可知,由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1.30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强;40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,增大压强平衡不移动,应是升高温度,故B正确;
C、由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1.则增大压强平衡不移动,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,则正反应为放热反应,故C错误;
D、40min时,改变条件平衡向逆反应方向移动,到达平衡时平衡常数减小,故D错误;
故选B.
A、反应从开始到8min内A浓度减少了0.64mol/L,根据v= ![]() 计算v(A);
计算v(A);
B.由图象可知,由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1.30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强;40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,则增大压强平衡不移动,应是升高温度;
C、由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1.则增大压强平衡不移动,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,则正反应为放热反应;
D、40min时,改变条件为升高温度,平衡常数发生变化.

【题目】汽车尾气是城市空气的主要污染物,如何减少汽车尾气(CO,NOx等)的污染是重要的科学研究课题.
(1)已知:N2(g)+O2(g)═2NO(g)△H1
N2(g)+3H2(g)2NH3(g)△H2
2H2(g)+O2(g)═2H2O(g)△H3
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=(用含△H1、△H2、△H3的式子表达)
(2)汽车尾气中的CO,NOx都需要除去,有人设想按下列反应除去CO;2CO(g)=2C(s)+O2(g)已知该反应在任何温度下都不能自发进行,因此该设想便不能实现.由此判断该反应的△H0
目前,在汽车尾气系统中装置催化转化器可以减少CO,NO的污染,其化学反应方程式为
(3)可用活性炭还原法处理氮氧化物.有关反应的化学方程式为:C(s)+2NO(g)N2(g)+CO2(g)△H>0某研究小组向密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
浓度/molL﹣1 | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
则,30min后,改变某一条件,平衡发生了移动,则改变的条件是;若升高温度,NO浓度将(填“增大”、“不变”或“减小”).
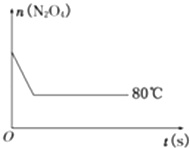
【题目】在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O42NO2 , 隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
n(N2O4) | 0.40 | a | 0.20 | c | d | e |
n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)计算20s一40s内用N2O4表示的平均反应速率为molL﹣1S﹣1;
(2)计算在80℃时该反应的平衡常数K=(请注明单位).
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”.“变深”或“不变”)
(4)要增大该反应的K值,可采取的措施有(填序号):
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线.