题目内容
3.设NA为阿伏加德罗常数,下列叙述正确的是( )| A. | 3.4gNH3中含有电子数为2NA | |
| B. | 0.1mol/L CuSO4溶液中含有的SO42-数目为0.1NA | |
| C. | 常温常压下,2.24L O3中含有的氧原子数为0.3NA | |
| D. | 足量的MnO2与50mL 8mol/L浓盐酸充分反应后,生成Cl2的分子数为0.1NA |
分析 A.每个NH3分子中含有10个电子;
B.溶液体积未知;
C.常温常压,Vm≠22.4L/mol;
D.只有浓盐酸与二氧化锰反应,稀盐酸不反应.
解答 解:A.n(NH3)=$\frac{3.4g}{17g/mol}$=0.2mol,含有的电子的物质的量为0.2mol×10=2mol,则个数为2NA,故A正确;
B.溶液体积未知,无法计算微粒个数,故B错误;
C.常温常压,Vm≠22.4L/mol,无法计算氧气的物质的量,故C错误;
D.足量的MnO2与50mL 8mol/L浓盐酸充分反应后,理论上生成0.1mol氯气,但是随着反应进行,盐酸浓度降低,稀盐酸与二氧化锰不反应,生成氯气小于0.1mol,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意气体摩尔体积的使用条件,注意二氧化锰与浓盐酸反应的条件,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列关于胶体的叙述中,不正确的是( )
| A. | 胶体中分散质粒子的直径小于1 nm | |
| B. | 胶体是一种介稳体系 | |
| C. | 用滤纸能分离胶体和悬浊液 | |
| D. | 利用丁达尔效应可以区分溶液和胶体 |
11.下列有关有机物的性质和应用正确的是( )
| A. | 天然气、石油都是清洁的可再生能源 | |
| B. | 乙烯和1,3-丁二烯互为同系物,它们均能使Br2水褪色 | |
| C. | 苯、乙醇和乙酸都能发生取代反应 | |
| D. | 石油的分馏可获得乙烯、丙烯等不饱和烃 |
15.下列叙述中,错误的是( )
| A. | 苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯 | |
| B. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| C. | 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 | |
| D. | 甲苯与氯气在光照下反应主要生成2-氯甲苯 |
12.在一定条件下能够发生水解反应,且水解的最终产物只有一种的是( )
| A. | 淀粉 | B. | 蚕丝 | C. | 豆油 | D. | 聚丙烯酸甲酯 |
13. 能源的发展日益成为全世界、全人类共同关心的问题.
能源的发展日益成为全世界、全人类共同关心的问题.
(1)A和B的单质单位质量的燃烧热大,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
①请根据上述信息,写出A基态原子的核外电子排布式:1s22s2.
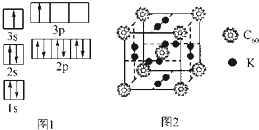
②某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了能量最低原理.
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.
①已知金刚石中C-C键的键长为154.45pm,C60中C-C键的键长为145pm和140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由不正确,C60是分子晶体,熔化时不需破坏化学键.
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.
③继C60后,科学家又合成Si60、N60,C、Si、N原子电负性由大到小的顺序是N>C>Si.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为30.
 能源的发展日益成为全世界、全人类共同关心的问题.
能源的发展日益成为全世界、全人类共同关心的问题.(1)A和B的单质单位质量的燃烧热大,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 899 | 1 757 | 14 840 | 21 000 |
| B | 738 | 1 451 | 7 733 | 10 540 |
②某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了能量最低原理.
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.
①已知金刚石中C-C键的键长为154.45pm,C60中C-C键的键长为145pm和140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由不正确,C60是分子晶体,熔化时不需破坏化学键.
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.
③继C60后,科学家又合成Si60、N60,C、Si、N原子电负性由大到小的顺序是N>C>Si.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为30.