题目内容
(15分)【化学---选修模块:物质结构与性质】
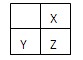
下表为周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是 (填编号)。
(2)元素⑥形成的最高价含氧酸根的立体构型是________,其中心原子的杂化轨道类型是_______。
(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是 。
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为 ;该元素与元素①形成的分子X构形为 ;X在①与③形成的分子Y中的溶解度很大,其主要原因是 。
(5)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为 (用对应的元素符号表示)。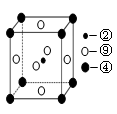
下表为周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是 (填编号)。
(2)元素⑥形成的最高价含氧酸根的立体构型是________,其中心原子的杂化轨道类型是_______。
(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是 。
| A.分子中含有氢键 | B.属于非极性分子 |
| C.含有4个σ键和1个π键 | D.该氢化物分子中,②原子采用sp2杂化 |
(5)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为 (用对应的元素符号表示)。

(1)⑨ (1分)
(2)正四面体(2分) SP3(2分) (3)B、D(2分)
(4)3 (2分) 三角锥形(2分) 在NH3分子和水分子间有氢键作用(2分)
(5)MgNi3C (2分)
(2)正四面体(2分) SP3(2分) (3)B、D(2分)
(4)3 (2分) 三角锥形(2分) 在NH3分子和水分子间有氢键作用(2分)
(5)MgNi3C (2分)
(1)区的名称来自按照构造原理最后通入电子轨道的能级名称,所以属于d区的是⑨,即镍元素。
(2)元素⑥是S,最高价氧化物的水化物是硫酸, SO42-硫原子的孤对电子是(6+2-2×4)÷2=0,即没有孤对电子,所以是正四面体,S原子是sp3杂化。
(3)产量作为衡量石油化工发展水平的标志是乙烯,乙烯分子中含有碳碳双键,但没有氢键、属于平面型结构,碳原子是sp2杂化。键角是120°,由于结构对称,所以是非极性分子。双键是由1个σ键和1个π键构成的,所以分子中含有5个σ键和1个π键,因此正确但答案选BD。
(4)根据核外电子的排布规律可知,s能级只能容纳2个电子,素n=2,即该元素是氮元素,核外最外层电子的孤对电子数为3。和氢元素形成氨气,是三角锥形结构。①与③形成的分子是水,由于在NH3分子和水分子间有氢键,且二者都是极性分子,所以氨气极易溶于水。
(4)④是镁,位于顶点,所以含有的原子个数是8×1/8=1,⑨是镍,位于面心处,含有6×1/2=3个。碳原子在中间,所以化学式为MgNi3C。
(2)元素⑥是S,最高价氧化物的水化物是硫酸, SO42-硫原子的孤对电子是(6+2-2×4)÷2=0,即没有孤对电子,所以是正四面体,S原子是sp3杂化。
(3)产量作为衡量石油化工发展水平的标志是乙烯,乙烯分子中含有碳碳双键,但没有氢键、属于平面型结构,碳原子是sp2杂化。键角是120°,由于结构对称,所以是非极性分子。双键是由1个σ键和1个π键构成的,所以分子中含有5个σ键和1个π键,因此正确但答案选BD。
(4)根据核外电子的排布规律可知,s能级只能容纳2个电子,素n=2,即该元素是氮元素,核外最外层电子的孤对电子数为3。和氢元素形成氨气,是三角锥形结构。①与③形成的分子是水,由于在NH3分子和水分子间有氢键,且二者都是极性分子,所以氨气极易溶于水。
(4)④是镁,位于顶点,所以含有的原子个数是8×1/8=1,⑨是镍,位于面心处,含有6×1/2=3个。碳原子在中间,所以化学式为MgNi3C。

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
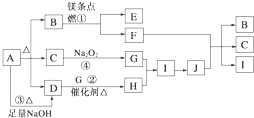
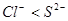 ②
②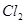 能与
能与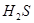 反应生成S
反应生成S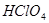 的酸性比
的酸性比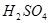 的强 ④常温下
的强 ④常温下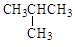 )的分子式相同
)的分子式相同