题目内容
同位素示踪法可用于反应机理的研究,下列有关反应中同位素示踪表示正确的是
| A.2Na218O2 + 2H2O=4Nal8OH + O2↑ |
| B.2KMnO4 + 5H218O2 + 3H2SO4=K2SO4 + 2MnSO4 + 518O2↑ + 8H2O |
C.NH4Cl + 2H2O NH3·2H2O + HCl NH3·2H2O + HCl |
| D.K37ClO3 + 6HCl=K37Cl + 3Cl2↑ + 3H2O |
B
解析试题分析:A、过氧化物与水反应实质为,过氧根离子结合水提供的氢离子生成过氧化氢,同时生成氢氧化钠,过氧化氢在碱性条件下不稳定,分解为水和氧气,所以18O同时在水中和氧气中,不出现在氢氧化钠中,故A错误;B、KMnO4中Mn元素化合价降低为2×(7-2)=10,H218O2中O元素化合价升高5×2×[0-(-1)]=10,化合价升降相等,高锰酸钾把过氧根氧化为氧气,18O全部在氧气中,故B正确;C、NH4Cl水解,其实是水电离的氢氧根、氢离子分别和NH4+、Cl-结合,生成一水合氨和氯化氢,所以2H应同时存在在一水合氨中和HCl中,故C错误;D、KClO3和HCl发生归中反应,KClO3中氯元素由+5价降低为0价,不能降低为-1,HCl中氯元素化合价由-1价升高为0价,氯气中的Cl有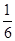 来自KClO3,
来自KClO3,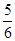 来自HCl,KCl中的Cl全部来自HCl,故D错误,答案选B。
来自HCl,KCl中的Cl全部来自HCl,故D错误,答案选B。
考点:考查氧化还原反应、盐类水解等反应原理的判断

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案一定要加入适当的氧化剂才能实现的转化是( )
| A.PCl3→PCl5 | B.MnO4- → Mn2+ | C.Na2O2→O2 | D.SO3→SO42- |
多硫化钠Na2Sx(x≥2)在结构上与Na2O2、FeS2、CaC2等有相似之处。Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,反应中Na2Sx与NaClO的物质的量之比为1︰16,则x的值是
| A.5 | B.4 | C.3 | D.2 |
下列关于置换反应:X+Y=W+Z(反应条件已经略去)的叙述正确的是( )
| A.若X是金属单质,则W和Z中一定有一种物质是金属单质 |
| B.若X是非金属单质,则W和Z中一定有一种物质是非金属单质 |
| C.若X是含有金属元素的化合物,则W和Z中一定有一种是含有金属元素的化合物 |
| D.若X是不含有金属元素的化合物,则W和Z中一定有一种物质是非金属单质 |
下列反应中,既能表现出硝酸的酸性,又能表现出其氧化性的是( )
| A.Fe2O3+HNO3 | B.NaOH+HNO3 |
| C.C+HNO3(浓) | D.Cu+HNO3 |
某氧化剂中,起氧化作用的是X2O72-离子,在溶液中0.2mol该离子恰好能使0.6mol的SO32-离子完全氧化,则X2O72-离子还原后X的化合价为
| A.+1 | B.+2 | C.+4 | D.+3 |
将0.195g锌粉加入到20mL 0.100 mol?L—1MO2+溶液中,恰好完全反应,则还原产物可能是
| A.M | B.M2+ | C.M3+ | D.MO2+ |
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。则下列说法错误的是
| A.反应过程中,被氧化与被还原的元素的物质的量之比为1:2 |
| B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 |
| C.若反应中转移的电子数目为6.02×1023,则可生成22.4L NO气体(标准状况) |
| D.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |