题目内容
向一个容积为4L的密闭容器中充入7molSO2和4molO2,在一定温度和压强下,发生如下反应:2SO2(g)+O2(g)

2SO3(g),经4s后达到平衡状态,测得SO2的物质的量是3mol,计算:
(1)以O2表示的该反应的速率______
(2)平衡时SO3的物质的量浓度______.

2SO3(g),经4s后达到平衡状态,测得SO2的物质的量是3mol,计算:
(1)以O2表示的该反应的速率______
(2)平衡时SO3的物质的量浓度______.
(1)以SO2表示的该反应的速率v(SO2)=
=0.25mol?L-1?s-1,速率之比等于化学计量数之比,所以有:
v(O2)=
v(SO2)=
×0.25mol?L-1?s-1=0.125mol?L-1?s-1;
故答案为:0.125mol?L-1?s-1
(2)参加反应的SO2的物质的量为7mol-3mol=4mol,根据方程式2SO2(g)+O2(g)?2SO3(g)可知,生成的SO3的物质的量等于参加反应的SO2的物质的量,平衡时SO3的物质的量浓度为c(SO3)=
=1mol/L.
故答案为:1mol/L
| ||
| 4s |
v(O2)=
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:0.125mol?L-1?s-1
(2)参加反应的SO2的物质的量为7mol-3mol=4mol,根据方程式2SO2(g)+O2(g)?2SO3(g)可知,生成的SO3的物质的量等于参加反应的SO2的物质的量,平衡时SO3的物质的量浓度为c(SO3)=
| 4mol |
| 4L |
故答案为:1mol/L

练习册系列答案
相关题目
 2SO3(g),经4s后达到平衡状态,测得SO2的物质的量是3mol,计算:
2SO3(g),经4s后达到平衡状态,测得SO2的物质的量是3mol,计算: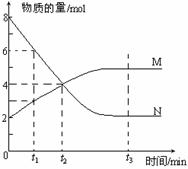 (2)在图上所示的三个时刻中, (填t1、t2或t3)时刻处于平衡状态,此时V正 V逆(填>、<或=,);达到平衡状态后,平均反应速率v(N)v(M)= 。
(2)在图上所示的三个时刻中, (填t1、t2或t3)时刻处于平衡状态,此时V正 V逆(填>、<或=,);达到平衡状态后,平均反应速率v(N)v(M)= 。 2SO3(g),经4s后达到平衡状态,测得SO2的物质的量是3mol,计算:
2SO3(g),经4s后达到平衡状态,测得SO2的物质的量是3mol,计算: