题目内容
11.S、D、W、Q分别代表四种元素,如果aSm+、bDn+、cWn-、dQm- 四种离子的电子层结构相同,则下列关系式正确的是( )| A. | a-b=n-m | B. | a-c=m+n | C. | c+d=m+n | D. | b-d=n-m |
分析 由aSm+、bDn+、cWn-、dQm-四种离子的电子层结构相同知,这四种离子的核外电子数相等,根据构成离子的原子序数、电荷数、质子数之间的可知得核外电子数=核内质子数-阳离子的电荷数=核内质子数+阴离子的电荷数,原子序数=核内质子数,所以得:a-m=b-n=c+n=d+m,以此来解答.
解答 解:由aSm+、bDn+、cWn-、dQm-四种离子的电子层结构相同知,这四种离子的核外电子数相等,得核外电子数=核内质子数-阳离子的电荷数=核内质子数+阴离子的电荷数,原子序数=核内质子数,所以得:a-m=b-n=c+n=d+m.
A、a-b=m-n,故A错误;
B、a-c=m+n,故B正确;
C、c-d=m-n,故C错误;
D、b-d=m+n,故D错误.
故选B.
点评 本题考查原子及离子结构,注意在离子的电子层结构相同的条件下,如果电荷的正负性相同,其原子序数之差=电荷数之差,如果电荷的正负性相反,其原子序数之差=电荷数之和.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1. 与等物质的量的Br2发生加成反应,生成的产物是( )
与等物质的量的Br2发生加成反应,生成的产物是( )
 与等物质的量的Br2发生加成反应,生成的产物是( )
与等物质的量的Br2发生加成反应,生成的产物是( )| A. | 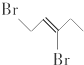 | B. | 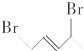 | C. |  | D. | 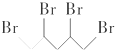 |
2.如图是四位同学学习了元素周期表后,对这节内容的认识,你认为不正确的是( )


| A. | A | B. | B | C. | C | D. | D |
19.下列“油”中属于酯类的是( )
①豆油 ②酱油 ③牛油 ④甘油 ⑤重油 ⑥硝化甘油.
①豆油 ②酱油 ③牛油 ④甘油 ⑤重油 ⑥硝化甘油.
| A. | ①③⑥ | B. | ②④⑤ | C. | ①③④ | D. | ③⑤⑥ |
16.下列不能用作喷泉实验的组合的是( )
| A. | HCl和水 | B. | 氨气和稀硫酸 | ||
| C. | 氯气和饱和食盐水 | D. | CO2和NaOH溶液 |
3.三聚氰胺又名蛋白精[分子式:C3N3(NH2)3,相对分子质量:126]是一种低毒性化工产品,婴幼儿大量摄入可引起泌尿系统疾患.有关三聚氰胺的下列说法正确的是( )
| A. | 2.52 g三聚氰胺含氮原子数目为0.12NA | |
| B. | 标准状况下1 mol的三聚氰胺的体积为22.4 L | |
| C. | 三聚氰胺含氮量约为10% | |
| D. | 三聚氰胺的摩尔质量为126 |
20.下列物质中既能发生氧化反应,又能发生还原反应的是( )
| A. | 甲醇 | B. | 乙酸 | C. | 甲醛 | D. | 乙酸乙酯 |
1.下列微粒中半径最小的( )
| A. | Na+ | B. | Cl- | C. | K+ | D. | S2- |


 .
. .
.