题目内容
用2.4mol/L的H2SO4溶液配制100mL浓度为0.2mol/L的稀H2SO4,回答下列问题:
(1)需用量筒量取2.4mol/L的H2SO4溶液的体积是______mL
(2)配制过程有下列几步操作:
A.用10mL量筒量取所需体积的H2SO4溶液,注入烧杯中,用玻璃棒搅拌,使其混合均匀;
B.将蒸馏水加入容量瓶至液面接近刻度线1cm~2cm处;
C.向烧杯中加入约20mL蒸馏水;
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液也转移到容量瓶中;
E.用______加水至刻度线;
F.将烧杯中溶液冷却后,沿玻璃棒转移到______;
G.盖好瓶塞,反复颠倒摇匀.
完成上述步骤,且以上各步骤操作的先后顺序是______(填字母)
(3)取上述所配溶液10mL与足量BaCl2溶液反应,生成白色沉淀0.48g.则该溶液浓度______0.2mol/L(填“大于”“等于”或“小于”),造成此误差的操作可能是______
A.定容时俯视容量瓶; B.用量筒取2.4mol/LH2SO4溶液时俯视读数;C.使用容量瓶前未干燥;D.使用的烧杯和玻璃棒未洗涤彻底;E.定容时将蒸馏水洒在容量瓶外面.
解:(1)根据稀释定律,稀释前后溶质硫酸的物质的量不变,设浓硫酸的体积为xmL,所以xmL×2.4mol/L=100mL×0.2mol/L,解得:x≈8.3,所以应量取的硫酸体积是8.3mL;
故答案为:8.3mL;
(2)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,用10mL量筒量取(用到胶头滴管)硫酸,在烧杯中稀释,并用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯与玻璃棒2~3次,并移入容量瓶内,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,盖好瓶塞,反复颠倒摇匀,故操作顺序为CAFDBEG;
故答案为:胶头滴管,100mL容量瓶,CAFDBEG;
(3)白色沉淀是硫酸钡,硫酸钡的物质的量为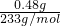 =
= mol,所以n(H2SO4)=n(BaSO4)=
mol,所以n(H2SO4)=n(BaSO4)= mol,故所配硫酸溶液的浓度为
mol,故所配硫酸溶液的浓度为 =0.21mol/L>0.2mol/L;
=0.21mol/L>0.2mol/L;
A.定容时俯视容量瓶,所配溶液体积偏小,配制人一样的浓度偏大,故A符合;
B.用量筒取2.4mol/LH2SO4溶液时俯视读数,量取硫酸溶液的体积偏小,所配溶液的浓度偏小,故B不符合;
C.配制需加水定容,使用容量瓶前未干燥,对所配溶液浓度无影响,故C不符合;
D.使用的烧杯和玻璃棒未洗涤彻底,移入容量瓶内溶质硫酸的物质的量偏小,所配溶液浓度偏小,故D不符合;
E.定容时将蒸馏水洒在容量瓶外面,可以继续加水,对所配溶液浓度无影响,故E不符合;
故答案为:大于,A.
分析:(1)根据稀释定律,稀释前后溶质硫酸的物质的量不变,据此计算需要硫酸的体积;
(2)根据配制溶液的实验操作过程进行步骤填空与实验步骤排序.
(3)白色沉淀是硫酸钡,根据n= 计算硫酸钡的物质的量,利用硫酸根守恒计算硫酸的物质的量,再根据c=
计算硫酸钡的物质的量,利用硫酸根守恒计算硫酸的物质的量,再根据c= 计算该硫酸溶液的浓度,据此判断;
计算该硫酸溶液的浓度,据此判断;
分析操作对溶质的物质的量或对溶液的体积的影响,根据c= 分析对所配溶液浓度的影响.
分析对所配溶液浓度的影响.
点评:本题考查了一定物质的量浓度溶液的配制,难度不大,注意从c= 理解溶液配制与误差分析.
理解溶液配制与误差分析.
故答案为:8.3mL;
(2)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,用10mL量筒量取(用到胶头滴管)硫酸,在烧杯中稀释,并用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯与玻璃棒2~3次,并移入容量瓶内,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,盖好瓶塞,反复颠倒摇匀,故操作顺序为CAFDBEG;
故答案为:胶头滴管,100mL容量瓶,CAFDBEG;
(3)白色沉淀是硫酸钡,硫酸钡的物质的量为
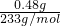 =
= mol,所以n(H2SO4)=n(BaSO4)=
mol,所以n(H2SO4)=n(BaSO4)= mol,故所配硫酸溶液的浓度为
mol,故所配硫酸溶液的浓度为 =0.21mol/L>0.2mol/L;
=0.21mol/L>0.2mol/L;A.定容时俯视容量瓶,所配溶液体积偏小,配制人一样的浓度偏大,故A符合;
B.用量筒取2.4mol/LH2SO4溶液时俯视读数,量取硫酸溶液的体积偏小,所配溶液的浓度偏小,故B不符合;
C.配制需加水定容,使用容量瓶前未干燥,对所配溶液浓度无影响,故C不符合;
D.使用的烧杯和玻璃棒未洗涤彻底,移入容量瓶内溶质硫酸的物质的量偏小,所配溶液浓度偏小,故D不符合;
E.定容时将蒸馏水洒在容量瓶外面,可以继续加水,对所配溶液浓度无影响,故E不符合;
故答案为:大于,A.
分析:(1)根据稀释定律,稀释前后溶质硫酸的物质的量不变,据此计算需要硫酸的体积;
(2)根据配制溶液的实验操作过程进行步骤填空与实验步骤排序.
(3)白色沉淀是硫酸钡,根据n=
 计算硫酸钡的物质的量,利用硫酸根守恒计算硫酸的物质的量,再根据c=
计算硫酸钡的物质的量,利用硫酸根守恒计算硫酸的物质的量,再根据c= 计算该硫酸溶液的浓度,据此判断;
计算该硫酸溶液的浓度,据此判断;分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
 分析对所配溶液浓度的影响.
分析对所配溶液浓度的影响.点评:本题考查了一定物质的量浓度溶液的配制,难度不大,注意从c=
 理解溶液配制与误差分析.
理解溶液配制与误差分析. 
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

