题目内容
下列叙述中,正确的是( )
分析:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物的反应放出的热量;
B、反应是可逆反应,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),不能进行完全,反应的焓变是对应化学方程式物质全部反应时放出的热量;
C、相同条件下,2mol氢原子结合为1mol氢分子的过程是放热反应;
D、反应自发进行的判断依据是△H-T△S,反应不能自发进行△H-T△S>0.
B、反应是可逆反应,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),不能进行完全,反应的焓变是对应化学方程式物质全部反应时放出的热量;
C、相同条件下,2mol氢原子结合为1mol氢分子的过程是放热反应;
D、反应自发进行的判断依据是△H-T△S,反应不能自发进行△H-T△S>0.
解答:解:A、甲烷燃烧的热化学方程式中水是气体,不符合燃烧热的概念,故A错误;
B、反应是可逆反应,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),不能进行完全,反应的焓变是对应化学方程式物质全部反应时放出的热量,故B错误;
C、相同条件下,2mol氢原子结合为1mol氢分子的过程是放热反应,所以2mol氢原子所具有的能量大于1mol氢分子所具有的能量,故C错误;
D、常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行△H-T△S>0,反应熵变大于0,T是常温下,所以判断△H>0,故D正确;
故选D.
B、反应是可逆反应,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),不能进行完全,反应的焓变是对应化学方程式物质全部反应时放出的热量,故B错误;
C、相同条件下,2mol氢原子结合为1mol氢分子的过程是放热反应,所以2mol氢原子所具有的能量大于1mol氢分子所具有的能量,故C错误;
D、常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行△H-T△S>0,反应熵变大于0,T是常温下,所以判断△H>0,故D正确;
故选D.
点评:本题考查了燃烧热的概念应用和判断,可逆反应与焓变的关系和含义,反应自发进行的判断依据,题目难度中等.

练习册系列答案
相关题目
下列叙述中不正确的是( )
| A、第ⅠA族的金属元素是同一周期中金属性最强的元素 | B、P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 | C、元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 | D、主族元素原子的最外层电子数不一定等于该元素的最高化合价 |
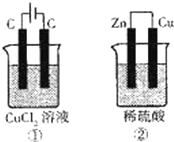 如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中不正确的是( )
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中不正确的是( )