题目内容
【题目】下列说法不正确的是( )
A.pH相等的四种溶液:![]()
![]()
![]()
![]() ,则四种溶液的溶质的物质的量浓度由小到大顺序为:
,则四种溶液的溶质的物质的量浓度由小到大顺序为:![]()
B.除去氯化铜溶液中的氯化铁杂质,可在溶液中加入过量的氧化铜,过滤达到除杂的目的
C.改变温度一定会导致已达化学平衡的反应发生移动
D.在一个固定容积的密闭容器中存在可逆反应![]() ,当混合气体的平均摩尔质量不再改变时,可逆反应一定达到平衡
,当混合气体的平均摩尔质量不再改变时,可逆反应一定达到平衡
【答案】D
【解析】
![]() 四种物质的水溶液均显碱性,同浓度时碱性强弱顺序为
四种物质的水溶液均显碱性,同浓度时碱性强弱顺序为![]() ,则等pH时四种溶液的溶质的物质的量浓度由小到大顺序为:
,则等pH时四种溶液的溶质的物质的量浓度由小到大顺序为:![]() ,故A正确;
,故A正确;
B. CuO可促进铁离子水解转化为沉淀,则加入过量的氧化铜,过滤达到除杂的目的,故B正确;
C. 化学反应中一定伴随能量变化,则改变温度一定会导致已达化学平衡的反应发生移动,故C正确;
D. 由质量守恒可知,气体的质量不变,若![]() 时,气体的物质的量始终不变,则混合气体的平均摩尔质量始终不变,不能判断可逆反应达到平衡,故D错误;
时,气体的物质的量始终不变,则混合气体的平均摩尔质量始终不变,不能判断可逆反应达到平衡,故D错误;
故选D。

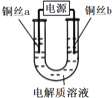
【题目】某小组同学用如下装置电解食盐水,并对电解产物进行探究。
实验装置 | 电解质溶液 | 实验现象 | |
|
| a极附近 | b极附近 |
开始时,产生白色浑浊并逐渐增加,当沉入U形管底部时部分沉淀变为橙黄色;随后a极附近沉淀自下而上也变为橙黄色 | 产生无色气泡 | ||
资料显示:
①氯化亚铜(CuCl)为白色粉末,微溶于水;
②氢氧化亚铜(CuOH)为黄色不溶于水的固体,易脱水分解为红色的![]() ;
;
③![]() 水溶液中不稳定,酸性条件下易歧化为
水溶液中不稳定,酸性条件下易歧化为![]() 和Cu;
和Cu;
④氢氧化铜可以溶于浓NaOH得到蓝色溶液.
![]() 经检验,b极产生的气体是
经检验,b极产生的气体是![]() ,b极附近溶液的pH______
,b极附近溶液的pH______![]() 填“增大”、“减小”、或“不变”
填“增大”、“减小”、或“不变”![]() ;铜丝a应与电源的______
;铜丝a应与电源的______![]() 填“正”或“负”
填“正”或“负”![]() 极相连。
极相连。
![]() 同学们分析a极附近生成的白色浑浊是CuCl,则该极的电极反应式是______。
同学们分析a极附近生成的白色浑浊是CuCl,则该极的电极反应式是______。
![]() ①橙黄色沉淀中含有
①橙黄色沉淀中含有![]() ,则CuCl转化为
,则CuCl转化为![]() 的原因是______
的原因是______![]() 用方程式表示
用方程式表示![]() ;
;
②结合离子在溶液中的运动规律,解释“
![]() 同学们通过实验进一步证实沉淀中含有
同学们通过实验进一步证实沉淀中含有![]() :将橙黄色沉淀滤出洗涤后,滴加
:将橙黄色沉淀滤出洗涤后,滴加![]()
![]() 至过量,应观察到的现象是______。
至过量,应观察到的现象是______。
![]() 同学们根据上述实验提出猜想:电解时,Cu做阳极先被氧化为
同学们根据上述实验提出猜想:电解时,Cu做阳极先被氧化为![]() 。为此,他们用Cu电极电解
。为此,他们用Cu电极电解![]() NaOH溶液,实验时观察到阳极产生大量无色气泡,附近溶液变蓝,未见预期的黄色沉淀。根据现象能否得出“该猜想不成立”的结论,并说明理由:______。
NaOH溶液,实验时观察到阳极产生大量无色气泡,附近溶液变蓝,未见预期的黄色沉淀。根据现象能否得出“该猜想不成立”的结论,并说明理由:______。
【题目】I .甲、乙、丙3位同学,在已知盐酸是强酸的基础上,通过实验验证醋酸是弱酸,分别设计了如下实验方案:
甲:分别准确配制0.1 mol/L的盐酸和醋酸各250 mL,再用pH试纸分别测定两溶液的pH。
乙:分别准确配制0.1 mol/L的盐酸和醋酸各250 mL。各取出20 mL于锥形瓶中,逐滴加入0.1 mol/L标准NaOH溶液(不需配制),分别记录恰好中和时用去NaOH溶液的体积。
丙:分别准确配制pH=1的盐酸和醋酸各250 mL。各取出10 mL加水稀释到100 mL后比较稀释后溶液的pH。回答下列问题:
(1)甲同学的实验结果为盐酸和醋酸的pH分别为pH1和pH2,则pH1_____pH2(填“>”“<”或“=”),所以此实验方案________(填“可行”或“不可行”)。
(2)乙同学的实验结果为盐酸和醋酸分别用去NaOH溶液V1 mL和V2 mL,则V1____V2(填“>”“<”或“=”),所以此实验方案______(填“可行”或“不可行”)。
(3)丙同学的实验方案不可行的原因是____________________________________。
II. 测定Na2S2O3样品纯度。
取10.0 g Na2S2O3·5H2O样品,配成 250mL溶液,准确量取25.00 mL溶液,以淀粉作指示剂,用0.1000 mol·L-1碘的标准溶液滴定。三次平行实验测得的数据如下:
实验序号 | 消耗标准溶液体积/mL |
1 | 19.98 |
2 | 17.90 |
3 | 18.10 |
已知:2Na2S2O3+I2=Na2S4O6+2NaI
①滴定终点的颜色为__________________。
②该Na2S2O3·5H2O样品的纯度为___%(保留2位小数)(已知Na2S2O3·5H2O的M=248g mol·-1)。
③若样品中含Na2SO3(还原性:SO32->I-),则测得的结果_______(填“偏高”“偏低”或“无影响”)
【题目】下面两表分别列出了CO和![]() 的某些性质及相关键能,有关说法不正确的是
的某些性质及相关键能,有关说法不正确的是
表1:
分子 | 熔点 | 沸点 | 常温时在水 中溶解度 |
CO |
|
|
|
|
|
|
|
表2:
CO |
|
|
|
键能 |
|
| |
|
|
|
|
键能 | 193 | 418 | 946 |
A.CO与![]() 的价电子总数相等
的价电子总数相等
B.由表2可知,CO的活泼性不及![]()
C.由表1可知,CO的熔沸点高于![]() ,是因为CO分子间作用力大于
,是因为CO分子间作用力大于![]()
D.由表1可知,室温时,CO在水中的溶解性大于![]() ,是因为CO分子有弱极性
,是因为CO分子有弱极性