题目内容
【题目】工业上利用硫酸废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)并回收(NH4)2SO4,具体生产流程如图所示:
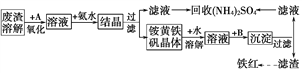
注:铵黄铁矾的化学式为(NH4)2Fe6(SO4)4(OH)12
回答下列问题:
(1)在废渣溶解操作中,加速废渣溶解的措施有________。
(2)物质A是一种氧化剂。
①工业上物质A最好选用________(填序号)。
A.空气 B.Cl2 C.MnO2 D.KMnO4
②简述工业上这样选择A的理由:__________________________________。
③写出A参与反应的离子方程式:__________________________________。
(3)往铵黄铁矾溶液(含Fe3+)中加入溶液B至pH为5时产生沉淀,请写出产生沉淀的离子方程式:__________________________________。
(4)回收所得的(NH4)2SO4晶体中可能含有的杂质是_______________________。
【答案】 不断搅拌、将废渣粉碎、升高温度(其他合理答案均可) A 成本或低价格低廉,且不带入杂质(其他合理答案均可) 4Fe2++O2+4H+===4Fe3++2H2O Fe3++3NH3·H2O===Fe(OH)3↓+3NH![]() MgSO4、CaSO4
MgSO4、CaSO4
【解析】废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO),将废渣溶解,溶解时加入的物质能溶解废渣但不能引进杂质;然后向溶液中加入A,A具有氧化性,能氧化亚铁离子但不能引进新的杂质且原料易得、成本低,应为空气中的氧气,然后向溶液中加入氨水,溶液中硫酸铁和氨水反应生成铵黄铁矾,同时溶液中镁离子、钙离子形成氢氧化钙、氢氧化镁、硫酸钙等会结晶析出,过滤分离得到铵黄铁矾和滤液;将滤液蒸发浓缩回收硫酸铵;将铵黄铁矾溶于水得到溶液,然后向溶液中加入氨水,得到氢氧化铁沉淀,然后过滤得到滤渣,将滤渣加热得到铁红。
(1)加速废渣溶解,可采用的措施有:将废渣粉碎、加热、搅拌等,故答案为:将废渣粉碎、加热、搅拌等;
(2)①物质A是氧化剂,具有氧化性,能氧化亚铁离子,但不能引进新的杂质且原料易得、成本低,氯气和二氧化锰都具有氧化性,但引进新的杂质且成本高,所以选取空气,故答案为:A;
②空气作为原料,成本低,不产生污染,不引入杂质,故答案为:原料易得,成本低,不产生污染,不引入杂质;
③氧化过程中发生反应的离子方程式为:4Fe2++O2+4H+═4Fe3++2H2O,故答案为:4Fe2++O2+4H+═4Fe3++2H2O;
(3)往铵黄铁矾溶液(含Fe3+)中加入氨水至pH为5时,铁离子与氨水反应生成氢氧化铁沉淀,反应的离子方程式为Fe3++3NH3·H2O===Fe(OH)3↓+3NH![]() ,故答案为:Fe3++3NH3·H2O===Fe(OH)3↓+3NH
,故答案为:Fe3++3NH3·H2O===Fe(OH)3↓+3NH![]() ;
;
(4)根据分析,回收所得的(NH4)2SO4晶体中可能含有的杂质有MgSO4、CaSO4,故答案为:MgSO4、CaSO4。

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】下列试剂中无法鉴别对应物质的是
选项 | 物质 | 试剂 |
A | 乙醛 甲苯和CCl4 | 水 |
B | 甲烷 乙炔和四氯化碳 | 溴水 |
C | 乙醇 乙酸和乙酸乙酯 | 饱和碳酸钠溶液 |
D | 苯甲醇 苯甲醛和苯甲酸 | 酸性高锰酸钾溶液 |
A. A B. B C. C D. D






