题目内容
下列关于原子结构、元素性质的说法正确的是( )
分析:A.元素周期律是指元素性质随原子序数的递增呈周期性变化;
B.电子层结构相同,核电荷数越大离子半径越小,最外层电子数相同电子层越多离子半径越大;
C.非金属性越强,气态氢化物越稳定,简单阴离子还原性越强,元素的非金属性越弱,据此判断;
D.同位素研究对象是原子,质子数相同中子数不同的原子互为同位素.
B.电子层结构相同,核电荷数越大离子半径越小,最外层电子数相同电子层越多离子半径越大;
C.非金属性越强,气态氢化物越稳定,简单阴离子还原性越强,元素的非金属性越弱,据此判断;
D.同位素研究对象是原子,质子数相同中子数不同的原子互为同位素.
解答:解:A.元素周期律是指元素性质随原子序数的递增呈周期性变化,故A错误;
B.第三周期元素的简单阳离子半径随原子序数的递增而减小,简单阴离子随原子序数的递增而减小,但阳离子半径小于阴离子半径,故B错误;
C.简单阴离子还原性越强,元素的非金属性越弱,非金属性越弱,气态氢化物的稳定性越弱,故C正确;
D.同位素研究对象是原子,16O2与18O2为同-物质,都是氧气,故D错误;
故选C.
B.第三周期元素的简单阳离子半径随原子序数的递增而减小,简单阴离子随原子序数的递增而减小,但阳离子半径小于阴离子半径,故B错误;
C.简单阴离子还原性越强,元素的非金属性越弱,非金属性越弱,气态氢化物的稳定性越弱,故C正确;
D.同位素研究对象是原子,16O2与18O2为同-物质,都是氧气,故D错误;
故选C.
点评:本题考查元素周期律、同位素、离子半径比较等,难度不大,注意D选项中16O2与18O2为同-物质,不是同素异形体.

练习册系列答案
相关题目
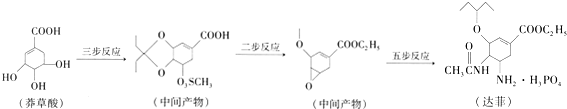
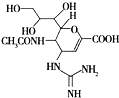
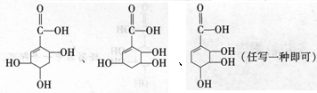

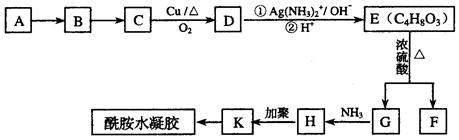
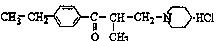
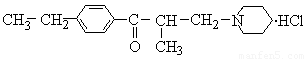 ,关于盐酸乙哌立松片有下列说法:
,关于盐酸乙哌立松片有下列说法: