题目内容
下列关于微粒结构的描述正确的是( )
分析:A.B.根据δ键和孤电子对数可判断分子的空间构型;
C.S原子最外层有6个电子,与6个F原子完全成键;
D.根据δ键和孤电子对数判断价层电子对数目可判断杂化类型.
C.S原子最外层有6个电子,与6个F原子完全成键;
D.根据δ键和孤电子对数判断价层电子对数目可判断杂化类型.
解答:解:A.CS2中含有2个δ键,没有孤对电子,则δ键为直线形分子,结构对称,为非极性分子,故A错误;
B.ClO3-中含有3个δ键,含有1个孤电子对,为三角锥形,故B错误;
C.S原子最外层有6个电子,与6个F原子完全成键,形成6个δ键,故C正确;
D.SiF4中含有4个δ键,为sp3杂化,SO32-中含有3个δ键,含有1个孤电子对,为sp3杂化,故D正确.
故选CD.
B.ClO3-中含有3个δ键,含有1个孤电子对,为三角锥形,故B错误;
C.S原子最外层有6个电子,与6个F原子完全成键,形成6个δ键,故C正确;
D.SiF4中含有4个δ键,为sp3杂化,SO32-中含有3个δ键,含有1个孤电子对,为sp3杂化,故D正确.
故选CD.
点评:本题考查较为综合,涉及分子构型和杂化类型的判断,题目难度中等,注意把握判断的方法,学习中注意积累.

练习册系列答案
相关题目

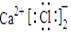 D.F原子结构示意:
D.F原子结构示意: