题目内容
7. (1)广州是一座美丽的海滨城市,海水资源非常丰富.海洋电池是以铝为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流,电池总反应为:4Al+3O2+6H2O═4A1(OH)3,下列说法正确的是bc(填写序号字母);
(1)广州是一座美丽的海滨城市,海水资源非常丰富.海洋电池是以铝为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流,电池总反应为:4Al+3O2+6H2O═4A1(OH)3,下列说法正确的是bc(填写序号字母);a.电池工作时,电流由铝电极沿导线流向铂电极
b.铂电极采用网状比块状更利于O2放电
c.海水中的OH向铝电极方向移动
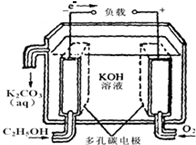
(2)乙醇是一种可再生能源,可用它来制成燃料电池(如图),试写出其负极的电极反应式C2H5OH-12e-+16OH-=2CO32-+11H2O
(3)高铁电池是一种新型可充电电池,比普通高能电池能保持稳定的放电电压.高铁电池的总反应为:
3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH.放电时负极反应为:Zn-2e-+2OH-═Zn(OH)2放电时正极附近溶液的碱性增强
(4)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐.电池反应方程式为C3H8+5O2═3CO2+4H2O;放电时CO32-移向电池的负(填“正”或“负”)极.
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为原料,以HCl-NH4Cl为电解质溶液制取新型燃料电池,同时达到固氮作用.该电池的正极反应式为N2+6e-+8H+=2NH4+
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极是负极(填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
分析 (1)根据电池总反应可知,电池工作时,负极为Al,发生氧化反应,电极反应式为Al-3e-+3OH-=Al(OH)3,正极上通入空气,发生还原反应,正极反应式为O2+2H2O+4e-=4OH-,结合原电池的工作原理解答该题;
(2)原电池中负极上燃料失电子,碱性条件下,CH3CH2OH反应生成碳酸根离子;
(3)根据电池总反应3Zn+2K2FeO4+8H2O═3Zn(OH)2+2Fe(OH)3+4KOH,可知,放电时,Zn被氧化,应为电池的负极,电极反应式为3Zn-6e-+6OH-═3Zn(OH)2,K2FeO4为电池的正极,发生还原反应,电极反应式为2FeO42-+6e-+8H2O═2Fe(OH)3+10OH-,结合电极反应式解答该题;
(4)燃料电池中,负极电极反应式为C3H8-20e-+10CO32-=13CO2+4H2O,正极反应式为:O2+2CO2+4e-=2CO32-,电解质溶液中阴离子向负极移动;
(5)N2在正极发生还原反应生成NH4+,以此书写电极反应式;
(6)(3)在燃料电池中,燃料做负极发生氧化反应,则通入氨气的电极是负极,碱性条件下,该电极发生反应的电极反应式为2NH3-6e-+6OH-→N2+6H2O.
解答 解:(1)a、电池工作时,电子由负极流向正极,即从铝电极沿导线流向铂电极,电流分析与电子移动分析相反,故a错误;
b、铂做成网状的目的是增大与氧气的接触面积,更利于O2放电,故b正确;
c、原电池中阴离子移向负极,所以海水中的OH-向铝电极方向移动,故c正确;
故答案为:bc;
(2)原电池中负极上燃料失电子,碱性条件下,CH3CH2OH反应生成碳酸根离子,电极反应式为C2H5OH-12e-+16OH-=2CO32-+11H2O,
故答案为:C2H5OH-12e-+16OH-=2CO32-+11H2O;
(3)放电时,Zn被氧化,生成Zn(OH)2,电极反应式为Zn-2e-+2OH-═Zn(OH)2,放电时,正极生成OH-,溶液碱性增强,
故答案为:Zn-2e-+2OH-═Zn(OH)2;增强;
(4)燃料电池中,负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应,负极电极反应式为C3H8-20e-+10CO32-=13CO2+4H2O,正极反应式为:O2+2CO2+4e-=2CO32-,所以其电池反应式为C3H8+5O2═3CO2+4H2O,放电时,电解质中阴离子碳酸根离子向负极移动,
故答案为:C3H8+5O2═3CO2+4H2O;负;
(5)N2在正极发生还原反应生成NH4+,电极反应式为N2+6e-+8H+=2NH4+,故答案为:N2+6e-+8H+=2NH4+;
(6)氨气在纯氧中燃烧,生成一种氮气和水,化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$ 2N2+6H2O,在燃料电池中,燃料做负极,则通入氨气的电极是负极,碱性条件下,该电极发生反应的电极反应式为2NH3-6e-+6OH-→N2+6H2O,
故答案为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$ 2N2+6H2O;负极;2NH3-6e-+6OH-=N2+6H2O.
点评 本题综合考查了原电池、电解池以及燃料电池的相关知识和电极反应式书写,题目综合性强,难度较大.

| A. | 第ⅠA族元素是同周期中金属性最强的金属元素 | |
| B. | 两个非金属原子间不可能形成离子键 | |
| C. | HF、HCl、HBr和HI的热稳定性和还原性依次减弱 | |
| D. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| A. | 用烧碱溶液消除制硝酸工业尾气的氮氧化物污染:NO2+NO+2NaOH═NaNO2+H2O | |
| B. | 制硝酸铜:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O | |
| C. | 制甲基丙烯酸甲酯(即有机玻璃):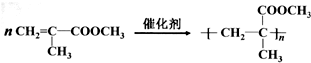 | |
| D. | 制硫酸铜:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,CuO+H2SO4(稀)═CuSO4+H2O |
| A. | AgCl不溶于水,不能转化为AgI | |
| B. | 两种难溶物的Ksp相差越大,难溶物就越容易转化为更难溶的物质 | |
| C. | AgI比AgCl更难溶于水,所以,AgCl可以转化为AgI | |
| D. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低 $\frac{1}{\sqrt{1.8}}$×10-11 mol•L-1 |
| A. | 18 g H2O中含有的质子数为10NA | |
| B. | 17g NH4+中含有的质子数为11NA | |
| C. | 46 g NO2和N2O4混合气体中含有的原子总数为3 NA | |
| D. | 1mol Na与足量的O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
| A. | 含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数为NA | |
| B. | 标准状况下,22.4 L O2 作氧化剂时转移电子数一定为4NA | |
| C. | 10 L 0.1 mol/L 的Na2CO3溶液中,Na+、CO32-总数为3NA | |
| D. | 通常状况下,4.2 g丙烯中所含碳氢键数目为0.6 NA |
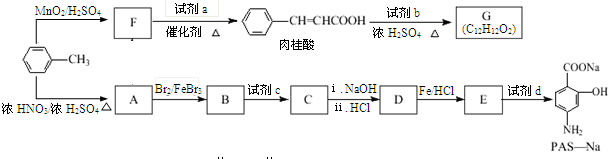
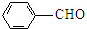 $→_{催化剂.△}^{RCH_{2}C-O-CCH_{2}R}$
$→_{催化剂.△}^{RCH_{2}C-O-CCH_{2}R}$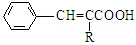 (R=CCOOH(R=-CH3或-H)
(R=CCOOH(R=-CH3或-H)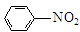 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$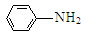
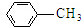 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$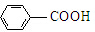
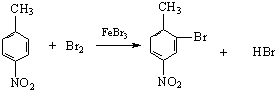 .
.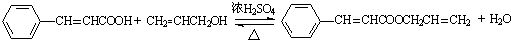 .
.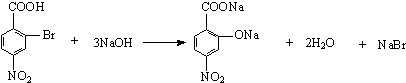 .
.