题目内容
下列化学实验事实及其解释都正确的是( )
| A、滴有酚酞的碳酸氢钠溶液呈浅红色,微热后红色加深,是因为碳酸氢钠分解生成了碳酸钠 |
| B、粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌含杂质 |
| C、纸层析法分离Fe3+和Cu2+的实验中,点样后的滤纸无需晾干就可将其浸入展开剂中 |
| D、向溴水中滴入植物油,振荡后,油层显无色,说明溴不溶于油脂 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.盐类水解是吸热反应,升高温度促进水解;
B.原电池加快金属被腐蚀;
C.晾干以保证每点在纸上扩散的直径不至于太大,否则各组分移动的时候会相互重叠;
D.油脂中含有不饱和键,溴能和不饱和键发生加成反应.
B.原电池加快金属被腐蚀;
C.晾干以保证每点在纸上扩散的直径不至于太大,否则各组分移动的时候会相互重叠;
D.油脂中含有不饱和键,溴能和不饱和键发生加成反应.
解答:
解:A.碳酸氢钠易水解,升高温度促进水解,溶液碱性增强,则溶液红色加深,故A错误;
B.粗锌中含有锌和其它杂质,锌、杂质和稀硫酸构成原电池,原电池加快金属被腐蚀,所以生成氢气反应速率加快,故B正确;
C.晾干以保证每点在纸上扩散的直径不至于太大,否则各组分移动的时候会相互重叠,导致分离不充分,影响实验结果,故C错误;
D.油脂中含有不饱和键,溴能和不饱和键发生加成反应而使溴水褪色,故D错误;
故选B.
B.粗锌中含有锌和其它杂质,锌、杂质和稀硫酸构成原电池,原电池加快金属被腐蚀,所以生成氢气反应速率加快,故B正确;
C.晾干以保证每点在纸上扩散的直径不至于太大,否则各组分移动的时候会相互重叠,导致分离不充分,影响实验结果,故C错误;
D.油脂中含有不饱和键,溴能和不饱和键发生加成反应而使溴水褪色,故D错误;
故选B.
点评:本题考查了实验方案评价,涉及盐类水解、原电池原理、加成反应等知识点,明确反应原理是解本题关键,知道油脂使溴水褪色和苯使溴水褪色原理不同,题目难度不大.

练习册系列答案
相关题目
一定条件下存在反应:A(g)+B(g)?C(g)+D(g)△H<0.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol A和1mol B,在Ⅱ中充入1mol C和1mol D,在Ⅲ中充入2mol A和2mol B,500℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C、容器Ⅰ中A的物质的量比容器Ⅱ中的多 |
| D、容器Ⅰ中A的转化率与容器Ⅱ中C的转化率之和小于1 |
既能与稀硫酸反应,又能与NaOH溶液反应,且都有气体放出的是( )
| A、NaHCO3 |
| B、(NH4)2CO3 |
| C、Al(OH)3 |
| D、Al2O3 |
0.1mol某金属和足量盐酸反应,产生0.15mol H2,该金属的核电荷数是( )
| A、11 | B、12 | C、13 | D、19 |
长周期元素周期表共有18个纵行,从左到右排为1~18列,即碱金属是第一列,稀有气体是第18列.按这种规定,下面说法不正确的是( )
| A、第9列元素中没有非金属 |
| B、第15列元素的原子最外层电子的排布是ns2np3 |
| C、最外层电子排布为ns2的元素都在第2列 |
| D、第10、11列元素分别处在d区和ds区 |
关于钠及其化合物性质的叙述,正确的是( )
| A、相同条件下,在水中碳酸钠的溶解度小于碳酸氢钠的溶解度 |
| B、氧化钠和过氧化钠都能与二氧化碳反应,生成物完全相同 |
| C、碳酸钠固体中混有少量碳酸氢钠,可用加热的方法除去 |
| D、质量相等的碳酸钠和碳酸氢钠分别与足量盐酸反应,后者产生气体少 |
如图是两种致癌物质的结构简式,以下的描述正确的是( )
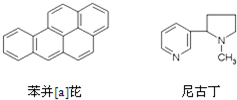

| A、它们都属于烃 |
| B、苯并[a]芘的分子式是C20H12 |
| C、尼古丁的分子式是C10H13N2 |
| D、苯并[a]芘的分子是由5个苯的结构单元并合而成,所以它是苯的同系物 |
下列叙述正确的是( )
| A、漂白粉和过氧化钠长期暴露在空气中最后均变质失效 |
| B、“低碳经济”就是要提倡大量使用煤、石油、天然气等化石燃料 |
| C、煤的干馏可以得到苯、甲苯等烃,不能得到衍生物 |
| D、只用淀粉溶液即可检验食盐是否为加碘盐 |
下列电离方程式中正确的是( )
| A、Na2HPO4溶于水:Na2HPO4=2Na++H++PO43- |
| B、NaHSO4熔化:NaHSO4=Na++H++SO42- |
| C、HF溶于少量水中:2HF=H++HF2- |
| D、(NH4)2 SO4溶于水:(NH4)2 SO4=2 NH4++SO42一 |