题目内容
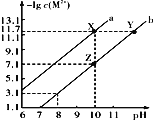
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgc(M2+)]与溶液pH的变化关系如图所示,已知该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2]。下列说法不正确的是( )
A. Ksp[Cu(OH)2]的数量级为10-20
B. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中c(Fe2+)∶c(Cu2+)=104.6∶1
C. 除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO
D. 向Z点对应的饱和溶液中加入少量NaOH固体,可转化为Y点对应的溶液
【答案】C
【解析】
25℃时,由Ksp[Cu(OH)2]<Ksp[Fe(OH)2]可知溶液pH相同时,饱和溶液中c(Fe2+) >c(Cu2+),则曲线a表示Cu(OH)2的饱和溶液中金属阳离子的物质的量浓度的负对数与溶液pH的变化关系,曲线b表示Fe (OH)2的饱和溶液中金属阳离子的物质的量浓度的负对数与溶液pH的变化关系。
A项、曲线a表示Cu(OH)2的饱和溶液中金属阳离子的物质的量浓度的负对数与溶液pH的变化关系,由图可知,当pH=10时,-lg c(M2+)=11.7,则Ksp[Cu(OH)2]= c(Cu2+) c2(OH-)= 10—11.7×(10—4)2=10—19.7,故A正确;
B项、当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中c(OH-)相同,当pH=10时,溶液中c(Fe2+)∶c(Cu2+)=10—7.1:10—11.7=104.6∶1,故B正确;
C项、该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2]可知,Cu(OH)2比Fe(OH)2更难溶,加入适量CuO调节溶液pH,先沉淀的是Cu2+,无法达到除去少量Fe2+的目的,故C错误;
D项、向Z点对应的饱和溶液中加入少量NaOH固体,溶液中c(OH-)增大,温度不变Ksp[Fe(OH)2],c(Fe2+)减小,可能由Z点转化为Y点,故D正确。
故选C。

 阅读快车系列答案
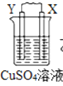
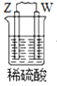
阅读快车系列答案【题目】由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
甲 | 乙 | 丙 | |
装置 |
|
|
|
现象 | 金属W不断溶解 | Y 的质量增加 | W上有气体产生 |
A.装置甲中W作原电池负极
B.装置乙中Y电极上的反应式为Cu2++2e=Cu
C.装置丙中溶液的c(H+)不变
D.四种金属的活动性强弱顺序为Z>W>X>Y