题目内容
13. 我国科学家屠呦呦因发现青蒿素治疗疟疾新疗法而获得2015年诺贝尔生理学或医学奖,已知青蒿素的结构简式如图.下列说法不正确的是( )
我国科学家屠呦呦因发现青蒿素治疗疟疾新疗法而获得2015年诺贝尔生理学或医学奖,已知青蒿素的结构简式如图.下列说法不正确的是( )| A. | 青蒿素可能具有强氧化性,具有杀菌消毒作用 | |
| B. | 青蒿素难溶于水,能溶于NaOH溶液 | |
| C. | 青蒿素分子中含有碳氧双键,但不能发生加成反应 | |
| D. | 青蒿素与纤维素一样,都属于有机高分子化合物 |
分析 由结构简式可知分子式,含酯基、醚键及过氧键,结合酯、过氧化物的性质来解答.
解答 解:A.含有过氧键,具有强氧化性,可用于杀菌消毒,故A正确;
B.含有酯基,难溶于水,可溶于氢氧化钠溶液,故B正确;
C.含有酯基,存在C=O键,与氢气不反应,故C正确;
D.高分子化合物的相对分子质量在10000以上,不是高分子化合物,故D错误.
故选D.
点评 本题考查有机物的结构和性质,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
4.在Na+浓度为0.5mol•L-1的某澄清溶液中,还可能含有K+、Ag+、Al3+、Ba2+、NO3-、CO32-、SO32-、SiO32-、SO42-等离子,取该溶液100mL进行如图连续实验(所加试剂均过量,气体全部逸出).下列说法不正确的是
( )

( )

| A. | 原溶液中一定不存在Ag+、Al3+、Ba2+、SO42- | |
| B. | 实验中生成沉淀的离子方程式是SiO32-+2H+=H2SiO3↓ | |
| C. | 原溶液一定存在K+、CO32-,可能存在NO3- | |
| D. | 原溶液不存在NO3-时,c(K+)=0.8mol•L-1 |
1.下列各组混合物无论以何种比例混合,只要总的物质的量一定,完全燃烧时消耗氧气的量是定值的是( )
| A. | C2H4、C2H5OH、HOCH2CH2COOH | B. | CH2O、C2H4O2、C6H12O6 | ||
| C. | C6H6、C5H10、C8H6O2 | D. | H2、CO、CH3OH |
18.化学与生活密切相关.下列有关说法错误的是( )
| A. | SiO2、MgO熔点高,可用于制作耐高温仪器 | |
| B. | 天然气是可再生清洁能源,可用于工业制盐酸 | |
| C. | 硝酸铵属于氧化剂,严禁用可燃物(如纸袋)包装 | |
| D. | 纤维素属于多糖类物质,但不能作人类的营养物质 |
5.设NA为阿伏加徳罗常数数值,下列有关叙述正确的是( )
| A. | 将78g Na2O2与过量CO2反应转移的电子数为2NA | |
| B. | 1molN2与4mol H2反应生成的NH3分子数为2NA | |
| C. | 标准状况下,2.24LCCl4中所含原子数为0.5NA | |
| D. | 标准状况下,18gD2O中所含电子数为9NA |
2.下列依据相关实验得出的结论正确的是.( )
| A. | 向新制的氯水中加入NaHCO3粉末,有气泡产生,说明氯元素的非金属性强于碳 | |
| B. | 向Fe(NO3)3溶液中通入适量SO2气体后,再滴加BaCl2溶液,产生白色沉淀,说明Fe3+能够将H2SO3氧化为H2SO4 | |
| C. | 向NaOH溶液中滴加少量的MgCl2溶液,产生白色沉淀,然后再滴加足量的CuCl2溶液,沉淀变蓝色,说明 Ksp[Cu(OH)2]<Ksp[Mg(OH)2] | |
| D. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈紫色,说明该溶液一定含有钾元素 |

 ;
;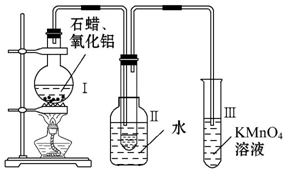 某研究性学习小组在实验室中模拟石油的催化裂化,装置如图,实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实验后闻试管Ⅱ中液体气味,具有汽油的气味.
某研究性学习小组在实验室中模拟石油的催化裂化,装置如图,实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实验后闻试管Ⅱ中液体气味,具有汽油的气味.