题目内容
下列实验原理、装置、试剂选用、结论正确的是
- A.用湿润的pH试纸测定稀盐酸的pH
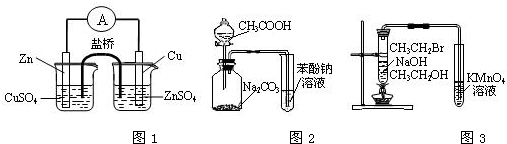
- B.用下图1构成锌-铜原电池
- C.用下图2根据有关实验现象推知酸性:CH3COOH>H2CO3>C6H5OH
- D.用下图3验证溴乙烷发生消去反应生成烯烃
C
分析:A.试纸湿润,测得盐酸的pH偏大;
B.左端烧杯发生置换反应,不能形成原电池;
C.根据强酸制取弱酸的反应原理来分析;
D.乙醇易挥发,且乙醇也能被高锰酸钾氧化.
解答:A.用湿润的pH试纸测定稀盐酸的pH,相当于盐酸稀释,测得盐酸的pH偏大,故A错误;
B.左端烧杯发生置换反应,整个装置不能形成电势差,则不能形成原电池,故B错误;
C.由醋酸和碳酸钠溶液反应生成碳酸,碳酸与苯酚钠溶液反应生成苯酚可知,酸性为CH3COOH>H2CO3>C6H5OH,故C正确;
D.乙醇易挥发,且乙醇也能被高锰酸钾氧化,则使高锰酸钾褪色的可能为乙醇,也可能为溴乙烷的消去产物(乙烯),故D错误;
故选C.
点评:本题考查实验方案的评价,明确pH的测定、原电池的形成、强酸制取弱酸的原理、有机物的性质即可解答,题目难度不大,选项B为易错点.
分析:A.试纸湿润,测得盐酸的pH偏大;
B.左端烧杯发生置换反应,不能形成原电池;
C.根据强酸制取弱酸的反应原理来分析;
D.乙醇易挥发,且乙醇也能被高锰酸钾氧化.
解答:A.用湿润的pH试纸测定稀盐酸的pH,相当于盐酸稀释,测得盐酸的pH偏大,故A错误;
B.左端烧杯发生置换反应,整个装置不能形成电势差,则不能形成原电池,故B错误;
C.由醋酸和碳酸钠溶液反应生成碳酸,碳酸与苯酚钠溶液反应生成苯酚可知,酸性为CH3COOH>H2CO3>C6H5OH,故C正确;
D.乙醇易挥发,且乙醇也能被高锰酸钾氧化,则使高锰酸钾褪色的可能为乙醇,也可能为溴乙烷的消去产物(乙烯),故D错误;
故选C.
点评:本题考查实验方案的评价,明确pH的测定、原电池的形成、强酸制取弱酸的原理、有机物的性质即可解答,题目难度不大,选项B为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目