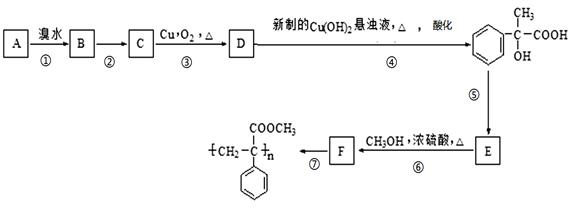
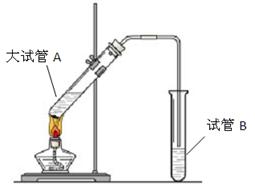
��Ŀ����
ij��ѧС���Ա�����Ϊԭ����ȡ������������й����ʵķе����Է������������
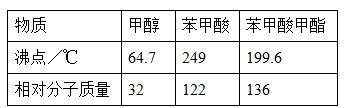
I.�ϳɱ���������ֲ�Ʒ
����ƿ�м���12.2g�������20mL�״����ܶ�Լ0.79g/mL�� ����С�ļ���3mL Ũ���ᣬ���Ⱥ�Ͷ�뼸�����Ƭ��С�ļ���ʹ��Ӧ��ȫ���ñ���������ֲ�Ʒ��
��1���÷�Ӧ��Ũ��������� ������Ӧ����ˮ��������ͬλ��18O��д���ܱ�ʾ��Ӧǰ��18Oλ�õĻ�ѧ����ʽ ���״�������ԭ�� ��
��2���������һ��ʱ��������Ǽ����Ƭ��Ӧ�ò�ȡ����ȷ������ ��
��3���ס��ҡ�����λͬѧ�ֱ��������ͼ����ʵ������ȡ�����������װ�ã��г������ͼ�������������ȥ���������л�����ص㣬��ò��� װ�ã���ס������ҡ�������������
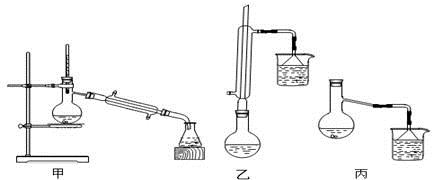
�ֲ�Ʒ�ľ���
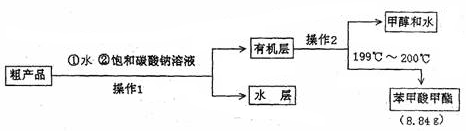
��4������������ֲ�Ʒ���������������״������ᡢ�������ˮ�ȣ���������������ͼ���о��ƣ����������ͼ����ǡ���������������ƣ�����IΪ ������IIΪ ��
��5����������ͼ�м���Na2CO3��Һ�����Һ©���������ã�Ҫ�õ��л��㣬���������� ��
��6������������IJ���Ϊ ��

I.�ϳɱ���������ֲ�Ʒ
����ƿ�м���12.2g�������20mL�״����ܶ�Լ0.79g/mL�� ����С�ļ���3mL Ũ���ᣬ���Ⱥ�Ͷ�뼸�����Ƭ��С�ļ���ʹ��Ӧ��ȫ���ñ���������ֲ�Ʒ��
��1���÷�Ӧ��Ũ��������� ������Ӧ����ˮ��������ͬλ��18O��д���ܱ�ʾ��Ӧǰ��18Oλ�õĻ�ѧ����ʽ ���״�������ԭ�� ��
��2���������һ��ʱ��������Ǽ����Ƭ��Ӧ�ò�ȡ����ȷ������ ��
��3���ס��ҡ�����λͬѧ�ֱ��������ͼ����ʵ������ȡ�����������װ�ã��г������ͼ�������������ȥ���������л�����ص㣬��ò��� װ�ã���ס������ҡ�������������

�ֲ�Ʒ�ľ���

��4������������ֲ�Ʒ���������������״������ᡢ�������ˮ�ȣ���������������ͼ���о��ƣ����������ͼ����ǡ���������������ƣ�����IΪ ������IIΪ ��
��5����������ͼ�м���Na2CO3��Һ�����Һ©���������ã�Ҫ�õ��л��㣬���������� ��
��6������������IJ���Ϊ ��
��1����������ˮ���� �÷�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�����������߲���
�÷�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�����������߲���
��2����ȴ��
��3����
��4����Һ������
��5������Һ©���ϿڵIJ���������ʹ���ϵİ��۶�©�����ϵ�С�ף�����������Һ©������������ƿ�����²�Һ�壬���²�Һ��պ�����ʱ�رջ��������л���ӷ�Һ©���Ͽڵ�����һ�ɾ������������ձ�����
��6��65 %
 �÷�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�����������߲���
�÷�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�����������߲�����2����ȴ��
��3����
��4����Һ������
��5������Һ©���ϿڵIJ���������ʹ���ϵİ��۶�©�����ϵ�С�ף�����������Һ©������������ƿ�����²�Һ�壬���²�Һ��պ�����ʱ�رջ��������л���ӷ�Һ©���Ͽڵ�����һ�ɾ������������ձ�����
��6��65 %
��1���״��ͱ�������Ũ�����������������¼��ȷ���������Ӧ�õ������������ˮ������Ũ��������ˮ�ԣ����շ�Ӧ������ˮ��ʹ������Ӧ��ƽ�������ƶ���������߷�Ӧ���ת���ʼ���Ʒ�IJ��ʡ������ڸ÷�Ӧ��Ũ���������������������ˮ����������Ӧ��ʵ���������ǻ������⡣���Ը÷�Ӧ�Ļ�ѧ����ʽΪ ���״�Ҫ��������Ϊ�÷�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�����������߲��ʡ���2���������һ��ʱ��������Ǽ����Ƭ��Ӧ��ֹͣ���ȣ���ȴ�����£����ٲ��ӡ�
���״�Ҫ��������Ϊ�÷�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�����������߲��ʡ���2���������һ��ʱ��������Ǽ����Ƭ��Ӧ��ֹͣ���ȣ���ȴ�����£����ٲ��ӡ�
��3������Ȼ��������ȴװ�ã����״��Ѿ������˷�Ӧ��ϵ������߷�Ӧ��������ʲ�������û����ȴ����װ�ã��ᵼ��һ���ַ�Ӧ�P����ӷ��ݳ��������ǶԻ������ǶԲ�Ʒ����ȡ�����������ҰѼס������ŵ㼯����һ�𣬼ȼ����˷�Ӧ��Ļӷ����ģ�Ҳ����˲�Ʒ�IJ��ʡ���ѡ����װ�á�
��4������������ֲ�Ʒ���������������״������ᡢ�������ˮ�ȣ��ȼ���ˮ�����ܽ����ᣬ�ټ��뱥�͵�Na2CO3��Һ���ȿ��Է�Ӧ���ı����ᣬҲ���Խ��ͱ�����������ܽ�ȡ����������ǻ������ݵ�Һ�壬��˿ɳ��÷�Һ�ķ������롣�ڷ�Һ�õ����л�������Ϊ�״��뱽��������ķе㲻ͬ��������ͨ��������뿪����
��5����Һ�ľ�������ǣ�����Һ©���ϿڵIJ���������ʹ���ϵİ��۶�©�����ϵ�С�ף�����������Һ©������������ƿ�����²�Һ�壬���²�Һ��պ�����ʱ�رջ��������л���ӷ�Һ©���Ͽڵ�����һ�ɾ������������ձ����С�
��6��n�������ᣩ="m/M=12.2g" ��122g/mol=0.1mol;n���״���=��20��0.79g�� ��32g/mol="15.8g��32g/mol" =0.494mol������������ʵ������㣬Ӧ���Ա�����Ϊ�������м��㡣n�������������=" m/M=8.84g��" 136g/mol="0.065mol." ����������IJ���Ϊ��0.065mol��0.1mol����100%="65" %
 ���״�Ҫ��������Ϊ�÷�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�����������߲��ʡ���2���������һ��ʱ��������Ǽ����Ƭ��Ӧ��ֹͣ���ȣ���ȴ�����£����ٲ��ӡ�
���״�Ҫ��������Ϊ�÷�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�����������߲��ʡ���2���������һ��ʱ��������Ǽ����Ƭ��Ӧ��ֹͣ���ȣ���ȴ�����£����ٲ��ӡ���3������Ȼ��������ȴװ�ã����״��Ѿ������˷�Ӧ��ϵ������߷�Ӧ��������ʲ�������û����ȴ����װ�ã��ᵼ��һ���ַ�Ӧ�P����ӷ��ݳ��������ǶԻ������ǶԲ�Ʒ����ȡ�����������ҰѼס������ŵ㼯����һ�𣬼ȼ����˷�Ӧ��Ļӷ����ģ�Ҳ����˲�Ʒ�IJ��ʡ���ѡ����װ�á�
��4������������ֲ�Ʒ���������������״������ᡢ�������ˮ�ȣ��ȼ���ˮ�����ܽ����ᣬ�ټ��뱥�͵�Na2CO3��Һ���ȿ��Է�Ӧ���ı����ᣬҲ���Խ��ͱ�����������ܽ�ȡ����������ǻ������ݵ�Һ�壬��˿ɳ��÷�Һ�ķ������롣�ڷ�Һ�õ����л�������Ϊ�״��뱽��������ķе㲻ͬ��������ͨ��������뿪����
��5����Һ�ľ�������ǣ�����Һ©���ϿڵIJ���������ʹ���ϵİ��۶�©�����ϵ�С�ף�����������Һ©������������ƿ�����²�Һ�壬���²�Һ��պ�����ʱ�رջ��������л���ӷ�Һ©���Ͽڵ�����һ�ɾ������������ձ����С�
��6��n�������ᣩ="m/M=12.2g" ��122g/mol=0.1mol;n���״���=��20��0.79g�� ��32g/mol="15.8g��32g/mol" =0.494mol������������ʵ������㣬Ӧ���Ա�����Ϊ�������м��㡣n�������������=" m/M=8.84g��" 136g/mol="0.065mol." ����������IJ���Ϊ��0.065mol��0.1mol����100%="65" %

��ϰ��ϵ�д�
 �������Ͽ��㱾ϵ�д�
�������Ͽ��㱾ϵ�д�
�����Ŀ
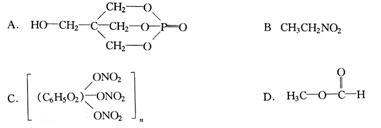
 ����1Ħ����˹ƥ�ֺ�������NaOH��Һ��ַ�Ӧ������NaOH�����ʵ���Ϊ
����1Ħ����˹ƥ�ֺ�������NaOH��Һ��ַ�Ӧ������NaOH�����ʵ���Ϊ