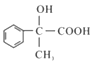
题目内容
【题目】利用下列实验装置完成相应的实验,能达到实验目的的是( )
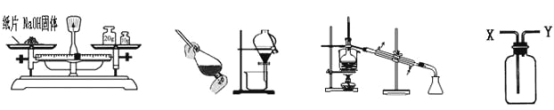
A. 称量NaOH固体 B. 用酒精提取溴水中的溴 C. 除去水中的氯化钠 D. 从Y进气收集CO2
【答案】C
【解析】
试题A.NaOH具有强腐蚀性且易潮解,为防止NaOH腐蚀仪器,所以NaOH应该放置在烧杯中称量,故A错误;B.萃取剂和原溶剂不能互溶,乙醇和水互溶,所以不能用乙醇作溴水的萃取剂,应该用苯或四氯化碳,故B错误;C.加热时,水易挥发,但NaCl不挥发,所以可以采用蒸馏方法除去水中的NaCl,故C正确;D.常温下和空气不反应且密度大于空气的气体采用向上排空气法收集,氯气密度大于空气且常温下和空气不反应,应该采用向上排空气法收集,导气管采用“长进短出”原则,故D错误。故选C。

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目