题目内容
【题目】水溶液X中只可能溶有K+、Mg2+、Al3+、AlO2﹣、SiO32﹣、SO32﹣、CO32﹣、SO42﹣中的若干种离子.某同学对该溶液进行了如图实验:下列判断正确的是( ) 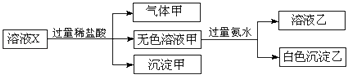
A.沉淀甲不一定是纯净物
B.溶液中一定有Al3+和CO32﹣和SiO32﹣
C.K+、AlO2﹣和SiO32﹣一定存在于溶液X中
D.CO32﹣和SO42﹣一定不存在于溶液X中
【答案】C
【解析】解:溶液X中进入过量盐酸,生成的气体甲,气体甲可能为二氧化硫或者二氧化碳,原溶液中可能存在SO32﹣、CO32﹣ , 溶液中一定不存在Mg2+、Al3+ , 再根据溶液电中性可知,原溶液中一定存在唯一的阳离子K+;
加入盐酸生成了沉淀甲,根据题干的离子可知,溶液中一定存在SiO32﹣ , 沉淀甲为硅酸;
无色溶液甲中加入过量氨水,得到的白色沉淀,说明原溶液中一定存在AlO2﹣ , 白色沉淀乙为氢氧化铝,
A.沉淀甲为硅酸,为纯净物,故A错误;
B.Al3+和CO32﹣、SiO32﹣发生互促水解反应,不能大量共存,故B错误;
C.根据以上分析可知,原溶液中一定存在K+、AlO2﹣和SiO32﹣ , 故C正确;
D.硫酸根离子是否存在不能确定,CO32﹣可能存在,故D错误.
故选C.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目