题目内容
9.6克元素A与4.2克元素B含有相同的原子数,A和B原子核中质子数与中子数相等,已知A元素在其最高价氧化物中的含量是40%,在其氢化物中含量为94.1%.试计算A、B两元素的相对原子质量,并推出他们在周期表中的位置.
考点:相对原子质量及其计算
专题:计算题
分析:令A元素最高正化合价为a,则最低负化合价为(a-8),A的相对分子质量为b,其最高价氧化物中A原子与O原子数目之比为2:a,由A元素在其最高价氧化物中的含量是40%,则2b:16a=40%:(1-40%),元素A的氢化物化学式为H(8-a)A,结合A元素质量分数列方程,联立方程可得A元素相对分子质量,进而计算B的相对分子质量,A和B原子核中质子数与中子数相等,相对原子质量-质子数+中子数,求出各自的质子数,确定元素的种类以及他们在周期表中的位置.
解答:
解:令A元素最高正化合价为a,则最低负化合价为(a-8),A的相对分子质量为b,
A元素最高价氧化物中A原子与O原子数目之比为2:a,由A元素在其最高价氧化物中的含量是40%,则2b:16a=40%:(1-40%),元素A的氢化物化学式为H(8-a)A,结合A元素质量分数可得:
=94.1%,联立方程,解得b=32,A原子核中质子数与中子数相等,相对原子质量-质子数+中子数,所以质子数为16,在周期表中第三周期ⅥA族;
令B元素相对分子质量为n,9.6g元素A与4.2g元素B含有相同的原子数,则
=
,解得n=14,B原子核中质子数与中子数相等,则B的质子数为7,为N元素,处于周期表中第二周期VA族,
答:A、B两元素的相对原子质量分别为:32、14,他们在周期表中的位置分别为:第三周期ⅥA族;第二周期VA族.
A元素最高价氧化物中A原子与O原子数目之比为2:a,由A元素在其最高价氧化物中的含量是40%,则2b:16a=40%:(1-40%),元素A的氢化物化学式为H(8-a)A,结合A元素质量分数可得:
| b |
| 8-a+b |
令B元素相对分子质量为n,9.6g元素A与4.2g元素B含有相同的原子数,则
| 9.6 |
| 32 |
| 4.2 |
| n |
答:A、B两元素的相对原子质量分别为:32、14,他们在周期表中的位置分别为:第三周期ⅥA族;第二周期VA族.
点评:本题考查元素推断、化学式有关计算,难度不大,注意掌握化学式中元素质量分数计算是解题的关键.

练习册系列答案
相关题目
下列说法中不正确的是( )
| A、摩尔是一种表示含有一定数目粒子集合体的物理量 |
| B、漂白粉、水玻璃、聚乙烯、福尔马林均为混合物 |
| C、硅单质常做半导体材料,二氧化硅则是制光导纤维的原料 |
| D、放热反应的化学反应速率不一定比吸热反应的反应速率快 |
下列有关叙述正确的是( )
| A、测定中和热时,大小两烧杯间填满碎纸的作用是固定小烧杯 |
| B、若用0.010mo1?L-1的氢氧化钠标准溶液滴定未知浓度的盐酸时,滴定前滴定管尖嘴处有气泡,滴定后气泡消失,则测定结果偏小 |
| C、在中和滴定实验中,滴定管用蒸馏水洗涤后,再用标准液润洗,再加进标准液 |
| D、进行中和滴定操作时,左手震荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化 |
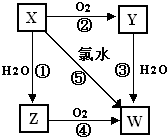 已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转化
已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转化
