题目内容
标准状况下,在三个干燥烧瓶一瓶为干燥纯净氨气,一瓶含一半空气的氯化氢和一瓶为二氧化氮和氧气的混合气(体积比:V(NO2):V(O2)=4:1),然后分别做喷泉实验,则三瓶中所得溶液的物质的量浓度之比为( )
| A.2:1:2 | B.5:5:4 | C.1:1:1 | D.无法确定 |
B
解析试题分析:假设烧瓶的容积为1L,则氨气的物质的量是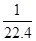 摩尔,溶液的体积是烧瓶的容积,则物质的量浓度是
摩尔,溶液的体积是烧瓶的容积,则物质的量浓度是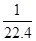 mol/L,含一半空气的氯化氢的物质的量是
mol/L,含一半空气的氯化氢的物质的量是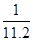 摩尔,溶液的体积是氯化氢的体积,即烧瓶容积的一半,则物质的量浓度是
摩尔,溶液的体积是氯化氢的体积,即烧瓶容积的一半,则物质的量浓度是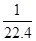 mol/L,二氧化氮和氧气的混合气(体积比:V(NO2):V(O2)=4:1),
mol/L,二氧化氮和氧气的混合气(体积比:V(NO2):V(O2)=4:1),
4NO2+O2+2H2O=4HNO3,硝酸的物质的量是NO2的物质的量,是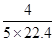 摩尔,溶液的体积是烧瓶容积,则物质的量浓度是
摩尔,溶液的体积是烧瓶容积,则物质的量浓度是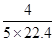 mol/L,所以比值是5:5:4,B正确。
mol/L,所以比值是5:5:4,B正确。
考点:考查喷泉实验、物质的量浓度计算

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
设NA表示阿伏加德罗常数,下列有关说法正确的是
| A.1.0 L 1 mol/L的NaNO3溶液中含有的氧原子数为3NA |
| B.30 g SiO2晶体中含有Si-O键数目为2NA |
| C.25℃时,pH=12的NaOH溶液中含有OH-的数目为0.01NA |
| D.1mol羟基与1molOH-离子所含电子数均为10NA |
下列叙述正确的是
| A.12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
| B.25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 NA |
| C.1mol的羟基与1 mol的氢氧根离子所含电子数均为9 NA |
| D.1.0L1.5mo1·L-1的NaAlO2水溶液中含有的氧原子数为3NA |
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O、NO+NO2+2NaOH=2NaNO2+H2O。则生成的盐溶液中NaNO3的物质的量为( )
| A.0.2 mol | B.0.4 mol | C.0.6 mol | D.0.8 mol |
据报道,科学家已成功合成了少量N4,有关N4的说法正确的是
| A.N4是N2的同素异形体 |
| B.N4是N2的同分异构体 |
| C.相同质量的N4和N2所含原子个数比为1:2 |
| D.N4的摩尔质量是56g |
设NA为阿伏加德罗常数的值,下列叙述不正确的( )
| A.10g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA |
| B.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C.50 mL 12 mol?L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| D.常温常压下,46g NO2 与N2O4的混合气体中含有的原子总数为3NA |
设NA表示阿伏加德罗常数,下列说法正确的是
| A.在常温常压下,11.2L N2含有的分子数为0.5NA |
| B.在常温常压下,18 g水中含有的分子数为NA |
| C.含有分子数为NA的氧气的质量是32g/mol |
| D.在2mol/L的MgCl2溶液中含有的Cl- 数为4NA |
设NA为阿伏伽德罗常数的数值,下列说法正确的是
| A.5.6g Fe与足量稀盐酸反应转移的电子数为0.3NA |
| B.常温常压下,23g NO2含有NA个氧原子 |
| C.标准状况下,22.4L水含有个NAH2O分子 |
| D.1mol/L NaCl溶液含有NA个Na+ |