题目内容
【题目】硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为0.2mol/L,硫酸根离子的浓度为0.5 mol/L,则混和溶液中镁离子浓度为( )。
A. 0.15 mol/L B. 0.3 mol/L C. 0.45 mol/L D. 0.2 mol/L
【答案】D
【解析】
根溶液显电中性分析解答。
混合溶液呈电中性,忽略水的电离,根据电荷守恒有2c(SO42-)=2c(Mg2+)+3c(Al3+),即:0.5mol/L×2=2c(Mg2+)+0.2mol/L×3,解得:c(Mg2+)=0.2mol/L,故答案选D。

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
【题目】某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol·L-1盐酸、0.55mol·L-1NaOH溶液,尚缺少的实验玻璃用品是______________、_________________。
实验用品 | 溶液温度 | 中和热△H | |||
t1 | t2 | ||||
① | 50mL0.55mol·L-1NaOH | 50mL.0.5mol·L-1HCl | 20℃ | 23.3℃ | _______ |
② | 50mL0.55mol·L-1NaOH | 50mL.0.5mol·L-1HCl | 20℃ | 23.5℃ | |
(2)他们记录的实验数据如下:
已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18kJ·℃-1·kg-1,各物质的密度均为lg·cm-3。计算完成上表。△H=____________
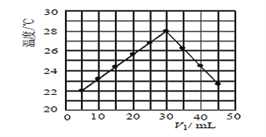
(3)某研究小组将V1mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2 =50mL)。此反应所用NaOH溶液的浓度应为__________mol/L。