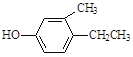题目内容
【题目】为了检验硫酸铵的热分解产物,某同学设计了如图所示实验装置。
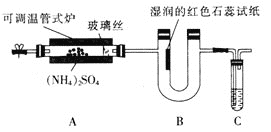
回答下列问题:
(1)![]() 装置A中玻璃丝的作用是________。
装置A中玻璃丝的作用是________。
![]() 若在
若在![]() 时加热,B中湿润的红色石蕊试纸变蓝,则有________(填化学式
时加热,B中湿润的红色石蕊试纸变蓝,则有________(填化学式![]() 产生;若C中盛放
产生;若C中盛放![]() 溶液,有白色沉淀产生,________(填“能”或“不能”
溶液,有白色沉淀产生,________(填“能”或“不能”![]() 说明分解产物中有
说明分解产物中有![]() ,理由是________________;若要检验是否有
,理由是________________;若要检验是否有![]() 产生,C中应盛放的试剂是________。
产生,C中应盛放的试剂是________。
(2)若在A中装入![]() ,按下图连接,在
,按下图连接,在![]() 时加热至完全分解。
时加热至完全分解。
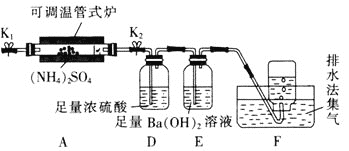
![]() 实验结束后,为防止倒吸,正确的操作是________。
实验结束后,为防止倒吸,正确的操作是________。
![]() 浓硫酸吸收的气体是________
浓硫酸吸收的气体是________![]() 填化学式
填化学式![]() 。
。
![]() 若D中增重
若D中增重![]() ,E中增重
,E中增重![]() ,F中收集的气体为
,F中收集的气体为![]() 已折算为标准状况
已折算为标准状况![]() ,分解反应的化学方程式为________。
,分解反应的化学方程式为________。![]() 已知分解产物中没有
已知分解产物中没有![]()
【答案】防止![]() 粉末进入后续装置
粉末进入后续装置 ![]() 不能
不能 ![]() 和
和![]() 同时通入
同时通入![]() 溶液中会生成
溶液中会生成![]() 沉淀 品红溶液 关闭
沉淀 品红溶液 关闭![]() ,打开
,打开![]()
![]() 、
、![]()
![]()
【解析】
(1)①装置A中玻璃丝的作用是防止![]() 粉末进入后续装置;
粉末进入后续装置;
②若在![]() 时加热,B中湿润的红色石蕊试纸变蓝,则有
时加热,B中湿润的红色石蕊试纸变蓝,则有![]() 产生,若C中盛放
产生,若C中盛放![]() 溶液,有白色沉淀产生,不能说明分解产物中有
溶液,有白色沉淀产生,不能说明分解产物中有![]() ,因为
,因为![]() 和
和![]() 同时通入
同时通入![]() 溶液中会生成
溶液中会生成![]() 沉淀;
沉淀;
(2)①实验结束后,应防止倒吸;
②![]() 分解产生
分解产生![]() 和
和![]() 可被浓硫酸吸收;
可被浓硫酸吸收;
③依据题给数据计算可得反应物的量,由此书写化学方程式。
(1)①装置A中玻璃丝的作用是防止![]() 粉末进入后续装置,故答案为:防止
粉末进入后续装置,故答案为:防止![]() 粉末进入后续装置;
粉末进入后续装置;
②若在![]() 时加热,B中湿润的红色石蕊试纸变蓝,则有
时加热,B中湿润的红色石蕊试纸变蓝,则有![]() 产生,若C中盛放
产生,若C中盛放![]() 溶液,有白色沉淀产生,不能说明分解产物中有
溶液,有白色沉淀产生,不能说明分解产物中有![]() ,因为
,因为![]() 和
和![]() 同时通入
同时通入![]() 溶液中会生成
溶液中会生成![]() 沉淀,可以用品红溶液检验
沉淀,可以用品红溶液检验![]() 气体,故答案为:
气体,故答案为:![]() ;不能;
;不能;![]() 和
和![]() 同时通入
同时通入![]() 溶液中会生成
溶液中会生成![]() 沉淀;品红溶液;
沉淀;品红溶液;
(2)①实验结束后,为防止倒吸,应关闭![]() ,打开
,打开![]() ,故答案为:关闭
,故答案为:关闭![]() ,打开
,打开![]() ;
;
②![]() 分解产生
分解产生![]() 和
和![]() ,浓硫酸能用来吸收
,浓硫酸能用来吸收![]() 和
和![]() ,故答案为:
,故答案为:![]() 、
、![]() ;
;
③![]() 硫酸铵的物质的量为
硫酸铵的物质的量为![]() ,D装置吸收氨气和水,E装置吸收二氧化硫,F装置收集的是氮气,故产生的
,D装置吸收氨气和水,E装置吸收二氧化硫,F装置收集的是氮气,故产生的![]() 为
为![]() ,
,![]() 为
为![]() ,
,![]() 的物质的量为
的物质的量为![]() ,根据N元素守恒,D装置中吸收的氨气为
,根据N元素守恒,D装置中吸收的氨气为![]() ,则D装置吸收的
,则D装置吸收的![]() 的物质的量为
的物质的量为![]() ,故该反应的化学方程式为:
,故该反应的化学方程式为:![]() ,故答案为:
,故答案为:![]() 。
。

【题目】现有五种有机物,请回答下列问题:
A. | B. | C. |
D.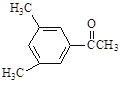 E.
E.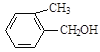 F.
F.![]()
(1)A物质中含有的官能团名称为_____________、______________。
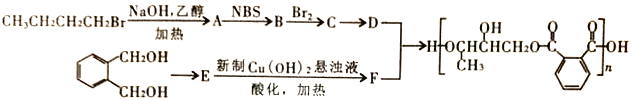
(2)B的分子式为_________________。
(3)D的一氯代物最多有________________种。
(4)上述化合物中互为同分异构体的是_____;互为同系物的是____。(填字母)