题目内容
【题目】某班化学兴趣小组做如下实验,请你回答相关问题:
Ⅰ、甲组同学想用金属钠和空气制备纯度较高的Na2O2(不考虑空气中N2),可利用的装置如下。回答下列问题:
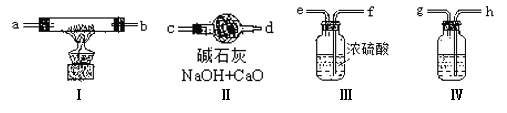
(1)装置Ⅳ中盛放的药品是 ,若没有该装置可能导致生成的Na2O2中含有 ,其反应方程式为 。
(2)若规定气体的气流方向从左到右,各仪器接口的标号字母(a、b……)顺序是:
空气进入 , 接 , 接 , 接 。
(3)装置的Ⅱ作用是 。
Ⅱ、乙组利用下图所示实验装置进行某些气体的制备、性质等试验(图中夹持装置有省略)。
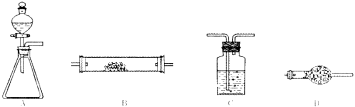
(4)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系。A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是 ;A中发生的化学方程式是 ,C中试剂是 ,D的作用是 。
【答案】(14分)(1)NaOH溶液(1分),Na2CO3(1分),2Na2O2+2CO2==2Na2CO3+O2↑(2分)
(2)h g f e a b c(2分)
(3)防止空气中的水分和二氧化碳倒吸进入装置Ⅰ(2分)
(4)浓盐酸(1分)(填“盐酸”可得分)
2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O(2分)(化学式写错、未配平均不得分。条件漏写扣1分。)浓硫酸(1分)吸收氯气以免污染环境(2分)(填“除去氯气”等合理答案可得分。)
【解析】
试题分析:(1)装置Ⅳ是利用NaOH溶液除去空气中的二氧化碳,若没有该装置,空气的CO2和Na2O2反应会生成碳酸钠,发生反应方程式为2Na2O2 +2CO2 == 2Na2CO3 + O2↑;
(2)依据上述分析确定连接顺序,组合实验装置时各仪器的正确连接顺序为Ⅳ、Ⅲ、Ⅰ、Ⅱ,根据气流方向各接口的连接顺序为h g f e a b c;
(3)利用装置Ⅱ中有碱石灰防止空气中的水分和二氧化碳倒吸进入装置Ⅰ;
(4)高锰酸钾和浓盐酸制备氯气,因此分液漏斗中为浓盐酸,发生反应的化学方程式为2KMnO4 + 16HCl(浓) = 2MnCl2 + 2KCl + 5Cl2↑ + 8H2O;氯气和水能反应生成HClO,HClO能使有色布条褪色,因此需要用浓硫酸干燥氯气;氯气有毒,不能直接排放到大气中,所以装置D是用于吸收氯气,以免污染环境。

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案