题目内容
【题目】碘酸钾(![]() )在生活中应用广泛,可将含碘物质经过系列变化得到
)在生活中应用广泛,可将含碘物质经过系列变化得到![]() .现向含
.现向含![]() 的稀硫酸中逐漓加入
的稀硫酸中逐漓加入![]() 溶液,整个过程中含碘物质的物质的量与加入
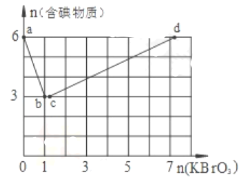
溶液,整个过程中含碘物质的物质的量与加入![]() 的物质的量的关系如图所示。回答下列问题:
的物质的量的关系如图所示。回答下列问题:
(1)已知![]() 段反应的离子方程式为
段反应的离子方程式为![]() b点时,KI恰好完全反应,则此时消耗的氧化剂与还原剂的物质的量之比是________还原产物是_______;共转移_______
b点时,KI恰好完全反应,则此时消耗的氧化剂与还原剂的物质的量之比是________还原产物是_______;共转移_______![]()
(2)![]() 过程中只有一种元素的化合价发生变化,写出该过程的离子方程式___________________从反应开始到达c点时,共消耗
过程中只有一种元素的化合价发生变化,写出该过程的离子方程式___________________从反应开始到达c点时,共消耗![]() ___________
___________![]()
【答案】1∶6 KBr 6 BrO3-+5Br-+6H+=3Br2+3H2O 1.2
【解析】
(1)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,根据I的物质的量变化规律可知该过程中I-被氧化成I2,KBrO3被还原成KBr,则KI为还原剂,KBrO3为氧化剂,则消耗的氧化剂与还原剂物质的量之比为1:6,还原产物是KBr,结合元素守恒和电子守恒可知a→b段反应方程式为:BrO3-+6I-+6H+=3I2+Br-+3H2O;1molKBrO3被还原成KBr,则转移6mol电子;
(2)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O;已知ab段发生反应BrO3-+6I-+6H+=3I2+Br-+3H2O,消耗KBrO3为1mol,则生成的Br-为1mol,根据bc段反应BrO3-+5Br-+6H+=3Br2+3H2O可知该段消耗KBrO3为0.2mol,则从反应开始到达c点时,共消耗n(KBrO3)=1mol+0.2mol=1.2mol。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目