题目内容
碳及其化合物应用广泛。
I.工业上利用CO和水蒸汽反应制氢气,存在以下平衡:CO(g)+H2O(g) 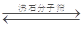 CO2(g)+H2(g)
CO2(g)+H2(g)
(1)沸石分子筛中含有硅元素,请写出硅原子结构示意图__________。
(2)向1L恒容密闭容器中注人CO和H2o(g),830℃时测得部分数据如下表。则该温度下反应的平衡常
数K=______________。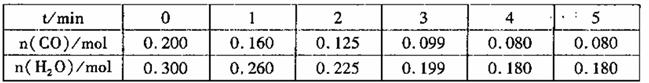
(3)相同条件下,向1L恒容密闭容器中,同时注人1mol CO、1mol H2O(g),2molCO2和2mo1 H2,此时v(正 ) __________v(逆)(填“>”“=”或“<”)
II.已知CO(g)+1/2 O2 (g)=CO2 (g) △H=一141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g) △H=一484 kJ·mol-1
CH3OH(1)+3/2O2 (g)=CO2(g)+2H2O(g) △Hl=一726 kJ·mol-1
(4)利用CO、H2化合制得液态甲醇的热化学方程式为___________。
III.一种新型氢氧燃料电池工作原理如下图所示
(5)写出电极A的电极反应式_____________。
(6)以上述电池电解饱和食盐水,若生成0.2mo1 Cl2,则至少需通人O2的体积为_____L(标准状况)。
(1)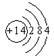 (2分)
(2分)
(2)1 (3分)
(3)< (2分)
(4)CO(g) + 2H2(g)=CH3OH(l) △H=+101 kJ/mol (方程式对给1分,共3分)
(5)H2-2e-+ CO32- =CO2 + H2O (3分) (6)2.24 (2分)
解析试题分析:(1)硅因素位于第三周期第ⅣA族,因此原子结构示意图为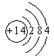 。
。
(2)根据表中数据可知,平衡时CO和水蒸气的浓度分别是0.080mol/L和0.180mol/L,其中消耗CO的浓度是0.200mol/L-0.080mol/L=0.120mol/L,因此根据方程式可知生成CO2和氢气的浓度均是0.120mol/L,实验该温度下反应的平衡常数K= =1。
=1。
(3)相同条件下,向1L恒容密闭容器中,同时注人1mol CO、1mol H2O(g),2molCO2和2mo1 H2,则此时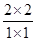 =4>1,所以反应逆反应方向进行,因此v(正 )<v(逆)。
=4>1,所以反应逆反应方向进行,因此v(正 )<v(逆)。
(4)已知① CO(g)+1/2 O2 (g)=CO2 (g) △H=一141 kJ·mol-1、② 2H2(g)+ O2(g)=2H2O(g) △H=一484 kJ·mol-1、③ CH3OH(1)+3/2O2 (g)=CO2(g)+2H2O(g) △Hl=一726 kJ·mol-1,则根据盖斯定律可知①+②-③即得到CO、H2化合制得液态甲醇的热化学方程式为CO(g) + 2H2(g)=CH3OH(l) △H=+101 kJ/mol。
(5)原电池中负极失去电子,发生氧化反应,正极得到电子发生还原反应。则根据装置图可知,氢气在A电极通入,因此A电极是负极,由于电解质是熔融的碳酸钾,而原电池中阴离子向负极移动,所以负极电极反应式为H2-2e-+ CO32- =CO2 + H2O。
(6)电解池中氯离子放电生成氯气,电极反应式为2Cl-2e-=Cl2↑,所以生成0.2mol氯气转移电子的物质的量是0.4mol。氧气在反应中得到4个电子,因此根据得失电子守恒可知消耗氧气的物质的量是0.4mol÷4=0.1mol,在标准状况下的体积是2.24L。
考点:考查原子结构示意图、平衡常数、热化学方程式、电化学原理的应用与有关计算

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案I.下面的虚线框中每一列、每一行相当于周期表的每一族和每一周期,但它的列数和行数都多于元素周期表。请在下面的虚线框中用实线画出周期表第1至第6周期的轮廓,并画出金属与非金属的分界线。
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
II.X、Y、Z、M、N为短周期的五种主族元素,其中X、Z同主族,Y、Z同周期,M与X、Y既不同周期,也不同族。X原子最外层电子数是核外电子层数的三倍,Y的最高价与最低价的代数和等于6。N是短周期主族元素中原子半径最大的非金属元素。
(1)X元素位于元素周期表第 周期,第 族;
N元素位于元素周期表第 周期,第 族。
(2)请写出下列反应的离子方程式:
N单质与氢氧化钠溶液反应:
(3)Y与Z相比,非金属性较强元素的原子结构示意图为 ,可以证明该结论的实验是(用离子方程式表示)
(4)请将X、Z、M、N元素原子半径从大到小排序:
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 | A | B | C | D |
| 性质结构信息 | 原子中最外层电子数为电子层数的2倍。常温下为淡黄色固体,其燃烧热为Q KJ/mol | 单质常温、常压下是气体,能溶于水。原子的M层p轨道有1个未成对的电子 | 单质质软、银白色固体、导电性强。单质在空气中燃烧发出黄色的火焰。 | 原子最外层电子层上s电子数等于p电子数。单质是一种重要的半导体材料。 |
(1)写出A的燃烧热方程式 。
(2)写出B单质与水反应的化学方程式 。
(3)电解B与C的化合物水溶液是重要化学工艺,写出离子方程式 。
(4)A与C形成的化合物存在的化学键为 (填“共价键”或“离子键”)。
(5)A、B、D三种元素电负性由小到大的顺序为 (写元素符号)。
(6)B、D两元素非金属性较弱的是 (写元素符号)。请设计一个实验证明这一结论: 。
A、B、C为短周期元素,在周期表中所处的位置如图所示。
| A | | C |
| | B | |
(1)写出A、B元素的名称________、________。
(2)B位于元素周期表中第________周期第________族。
(3)C的原子结构示意图为________。
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式________________________________________________________________。
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
| 周期 | ⅠA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | | | ⑦ | ⑧ | |
(1)请画出元素⑥的离子结构示意图: 。
(2)元素⑦中质子数和中子数相等的同位素符号是: 。
(3)④、⑤、⑦的离子半径由大到小的顺序为: 。
(4)②的最高价氧化物对应水化物的电离方程式为: 。
(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为: 。
(6)由表中两种元素形成的5核10电子分子常做燃料电池的燃料,该电池在碱性条件下的负极反应式为: 。
(7)由表中两种元素形成的氢化物A和B都含有18个电子,A是一种6原子分子,可做火箭发动机燃料;B是一种常见强氧化剂。已知16g液态A与液态B充分反应生成一种液态10电子分子和一种气态单质,并放出838kJ热量,写出A与B反应的热化学方程式: 。
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N元素的电负性由大到小的顺序是___________________,
C60和金刚石都是碳的同素异形体,二者相比,熔点高的是________,原因是____________________________。
(2)A、B均为短周期金属元素,依据表中数据,写出B的基态原子的电子排布式:________________。
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,d0或d10排布无颜色,d1~d9排布有颜色。如[Co(H2O)6]2+显粉红色。据此判断:[Mn(H2O)6]2+________(填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为
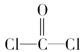 ,每个COCl2分子内含有________个σ键,________个π键,其中心原子采取________杂化轨道方式。
,每个COCl2分子内含有________个σ键,________个π键,其中心原子采取________杂化轨道方式。②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)。反应过程中,断裂的化学键只有配位键,则形成的化学键类型是________。
