题目内容
15.碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.Ⅰ、制备
碱式碳酸铜因生成条件不同,其颜色和组成也不尽相同,即碱式碳酸铜中Cu(OH)2和CuCO3的比例不同,某实验小组设计以下不同实验制备碱式碳酸铜.
(1)由Na2CO3•10H2O与CuSO4•5H2O反应制备:称取14g CuSO4•5H2O、16g Na2CO3•10H2O,用研钵分别研细后再混合研磨,立即发生反应,有“嗞嗞”声,而且混合物很快成为“粘胶状”,将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀产生,过滤,用水洗涤沉淀,至滤液中不含SO42-为止,取出沉淀,风干,得到蓝绿色晶体.
①混合物发生反应时有“嗞嗞”声的原因是有CO2气体生成,混合物成为“粘胶状”的原因是混合物吸水;
②撤离热源的目的是防止碱式碳酸铜受热分解;
③检验滤液中是否含有SO42-的方法是首先在滤液中加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-,否则没有;
(2)由Na2CO3溶液与CuSO4溶液反应制备:分别按一定比例取CuSO4溶液和Na2CO3溶液,水浴加热到设定温度后,在充分振荡下采用将CuSO4溶液加入Na2CO3溶液或将Na2CO3溶液加入CuSO4溶液的加料顺序进行实验,影响产品组成和产率的因素可能有温度、反应物配比、溶液酸碱度(列2点).
分析 (1)①用研钵分别研细后再混合研磨,发生水解反应,有CO2气体生成,产生大量气泡,有“磁磁”的声音,而且混合物吸湿很厉害,很快成为“粘胶状;
②碱式碳酸铜受热容易分解;
③在滤液中加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-;
(2)产物的组成与反应物配比、溶液酸碱度、温度等有关,从而使碱式碳酸铜中Cu(OH)2和CuCO3的比例不同.
解答 解:(1)①用研钵分别研细后再混合研磨,发生水解反应,有CO2气体生成,产生大量气泡,所以会有“磁磁”的声音,由于混合物易吸水,很快成为“粘胶状,
故答案为:有CO2气体生成;混合物吸水;
②由于碱式碳酸铜受热容易分解,故应迅速撤离热源,防止其分解,
故答案为:防止碱式碳酸铜受热分解;
③滤液中是否含有SO42-的操作方法是:首先在滤液中加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-,否则没有,
故答案为:首先在滤液中加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-,否则没有;
(2)产物的组成与反应物配比、溶液酸碱度、温度等有关,从而使碱式碳酸铜中Cu(OH)2和CuCO3的比例不同,
故答案为:反应物配比、溶液酸碱度等.
点评 本题考查制备实验方案,侧重对实验现象的分析、问题讨论的考查,综合考查学生对知识的迁移应用,难度中等.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
5.下列说法正确的是( )
| A. | 用BaCl2 溶液可证明Na2CO3溶液显碱性时由于CO32-发生水解 | |
| B. | NaHCO3 溶液中存在:c(Na+ )=c(HCO3-)+c(CO3 2-) | |
| C. | CH3COOH溶液中加入少量CH3COONa 固体后溶液中c(H+)•c(CH3COO-)增大 | |
| D. | 相同温度下,Ksp较小的物质其溶解度也一定较小 |
6.下列烷烃的一氯代物中没有同分异构体的是( )
| A. | 丁烷 | B. | 丙烷 | C. | 乙烷 | D. | 2-甲基丙烷 |
7.下列表示丙基的是( )
| A. | CH3CH2CH3 | B. | CH3CH2CH2- | C. | -CH2CH2- | D. | CH3- |
13.分子式为C5H12的烷烃的一氯取代物共有( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
14.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: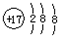 | B. | 氯化铵的电子式: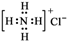 | ||
| C. | CO2的结构式:O=C=O | D. | CH4的比例模型: |
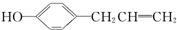
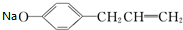 +H2O;
+H2O;