题目内容
下列化学用语正确的是( )
| A、C2H2分子的结构式:H-C≡C-H |
| B、NaH与重水反应的方程式:NaH+D2O=NaOH+D2↑ |
C、S2-的结构示意图: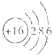 |
D、二氧化碳的电子式: |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.乙炔分子中存在碳碳三键,将电子式中的共用电子对换成短线,即为结构式;
B.NaH与重水发生氧化还原反应,根据氧化还原反应中同种元素的化合价向中间靠拢原则,NaH 中H显-1价,与水反应后生成0价的氢气;
C.硫离子的核外电子总数为18,最外层为8个电子;
D.二氧化碳分子中存在两个碳氧双键,碳原子和氧原子都达到8电子稳定结构.
B.NaH与重水发生氧化还原反应,根据氧化还原反应中同种元素的化合价向中间靠拢原则,NaH 中H显-1价,与水反应后生成0价的氢气;
C.硫离子的核外电子总数为18,最外层为8个电子;
D.二氧化碳分子中存在两个碳氧双键,碳原子和氧原子都达到8电子稳定结构.
解答:
解:A.乙炔为共价化合物,分子中存在一个碳碳三键和两个碳氢键,为直线型结构,乙炔的结构式为:H-C≡C-H,故A正确;
B.NaH与重水的反应中,NaH中-1价H变成了0价的氢气,正确的化学方程式:NaH+D2O=NaOD+HD↑,故B错误;
C.硫离子的核电荷数为16,核外电子总数为18,硫离子的结构示意图为: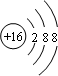 ,故C错误;
,故C错误;
D.二氧化碳为共价化合物,分子中存在2个碳氧双键,二氧化碳的电子式为: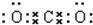 ,故D错误;
,故D错误;
故选A.
B.NaH与重水的反应中,NaH中-1价H变成了0价的氢气,正确的化学方程式:NaH+D2O=NaOD+HD↑,故B错误;
C.硫离子的核电荷数为16,核外电子总数为18,硫离子的结构示意图为:
 ,故C错误;
,故C错误;D.二氧化碳为共价化合物,分子中存在2个碳氧双键,二氧化碳的电子式为:
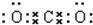 ,故D错误;
,故D错误;故选A.
点评:本题考查了电子式、离子结构示意图、氧化还原反应方程式书写的判断,题目难度中等,注意掌握常见化学用语的概念及书写方法,选项B为易错点,注意NaH中H元素的化合价为-1价,反应后变成0价.

练习册系列答案
相关题目
LiH是一种氢气发生剂,用于军事或其他需氢气的场合.反应为:LiH+H2O→LiOH+H2↑在这个反应中( )
| A、是非氧化还原反应 |
| B、每1摩尔LiH参与反应,电子转移2摩尔 |
| C、H2既是氧化产物,又是还原产物 |
| D、LiH既是氧化剂,又是还原剂 |
 甲装置中所含的是物质的量之比为1:2的CuSO4和NaCl的混合溶液,电解过程中溶液的pH值随时间t变化的示意图如乙示(不考虑电解产物可能与水的反应).试分析下列叙述中正确的是( )
甲装置中所含的是物质的量之比为1:2的CuSO4和NaCl的混合溶液,电解过程中溶液的pH值随时间t变化的示意图如乙示(不考虑电解产物可能与水的反应).试分析下列叙述中正确的是( )| A、该混合溶液中的SO42-导致了A点溶液的pH值小于B点 |
| B、AB线段与BC线段在阴极上发生的反应是相同的,即:Cu2++2e-→Cu |
| C、BC段阴极产物和阳极产物的体积之比为2:1 |
| D、在整个电解的过程中会出现少量淡蓝色的Cu(OH)2沉淀 |
下列有关金属的保护方法的说法中正确的是( )
| A、常使用的快餐杯表面有一层搪瓷,搪瓷层破损后仍能起到防止生锈的作用 |
| B、白铁(镀锌铁)镀层破损后,铁皮的腐蚀速度很慢 |
| C、轮船的船壳水线以下常装有一些锌块,这是利用了牺牲阴极的阳极保护法 |
| D、钢铁制造的暖气管道外常涂有一层沥青,这是钢铁的电化学保护法 |
某溶液中含有较多的AlO2-,则溶液中可能存在的离子组合是( )
| A、Al3+、NO3-、SO42- |
| B、Mg2+、SO42-、OH- |
| C、H+、NH4+、Cl- |
| D、Na+、Cl-、OH- |
第85号元素砹(At)是核电荷数最大的卤素,下列关于砹及其化合物的叙述中正确的是( )
| A、At2可能是一种有色固体,难溶于水,易溶于有机溶剂 |
| B、AgAt见光易分解,是一种能溶于水的有色固体 |
| C、相同条件下,HAt比HI更稳定 |
| D、由KAt的水溶液制备砹的化学方程式为:2KAt+Cl2→2KCl+At2 |
盛装无水乙醇的试剂瓶上贴有的标识是( )
A、 |
B、 |
C、 |
D、 |