题目内容
【题目】Ⅰ.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
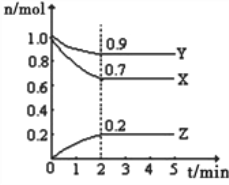
(1)反应开始至2min,以气体Z表示的平均反应速率为______________________;
(2)平衡时容器内混合气体密度比起始时__________(填“变大”,“变小”或“相等”下同),混合气体的平均相对分子质量比起始时___________;
(3)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=___________。
Ⅱ.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比。
(1)一定能证明2SO2(g)+O2(g)![]() 2SO3(g)达到平衡状态的是_______(填序号)
2SO3(g)达到平衡状态的是_______(填序号)
(2)一定能证明I2(g)+H2(g)![]() 2HI(g)达到平衡状态的是 _________。(填序号)
2HI(g)达到平衡状态的是 _________。(填序号)
(3)一定能证明A(s)+2B(g)![]() C(g)+D(g)达到平衡状态的是________。(注:B,C,D均为无色物质)
C(g)+D(g)达到平衡状态的是________。(注:B,C,D均为无色物质)
【答案】0.01mol/(L·min)相等变大7:5①③④⑤②④
【解析】
I.(1)v(Z)=0.2/(2×10)mol/(L·min)=0.01 mol/(L·min),故答案为:0.01 mol/(L·min);
(2)组分都是气体,容积不变,因此反应前后气体密度不变,根据M=m/n,组分都是气体,气体质量不变,向正反应方向进行,气体物质的量减小,则M增大;故答案为:相等、变大;
(3)设转化的X为3x,由三段式分析如下:
3X + Y![]() 2Z
2Z
起始: a b 0
变化: 3x x 2x
某时刻:a-3x b-x 2x
n(X)=n(Y)=2n(Z),因此有a-3x=b-x,a-3x=4x,a=7x,b=5x,因此a:b=7x:5x=7:5;故答案为:7:5;
II.(1)①反应前后气体系数之和不相等,因此压强不变,说明反应达到平衡,故①正确;②组分都是气体,气体质量不变,是恒容状态,容器的体积不变,因此密度不变,不能说明反应达到平衡,故②错误;③向正反应方向进行,气体物质的量减少,因此总物质的量不变,说明反应达到平衡,故③正确; ④根据M=m/n,组分都是气体,气体质量不变,向正反应方向进行,气体物质的量减小,因此当M不变,说明反应达到平衡,故④正确;⑤组分都是无色气体,因此颜色不变,不能说明反应达到平衡,故⑤错误;⑥没有指明反应进行方向,故⑥错误;故答案为:①③④;
(2)①反应前后气体系数之和相等,因此压强不变,不能说明反应达到平衡,故①错误;②组分都是气体,气体质量不变,是恒容状态,容器的体积不变,因此密度不变,不能说明反应达到平衡,故②错误;③反应前后气体系数之和相等,因此物质的量不变,不能说明反应达到平衡,故③错误; ④根据M=m/n,组分都是气体,气体质量不变,气体总物质的量不变,因此当M不变,不能说明反应达到平衡,故④错误;⑤I2是有颜色的气体,因此颜色不变,说明反应达到平衡,故⑤正确;⑥没有指明反应进行方向,故⑥错误;故答案为:⑤;
(3)①反应前后气体系数之和相等,因此压强不变,不能说明反应达到平衡,故①错误;②A为固体,其余为组分都是气体,气体质量增加,是恒容状态,容器的体积不变,因此密度不变,说明反应达到平衡,故②正确;③气体物质的量不变,因此总物质的量不变,不能说明反应达到平衡,故③错误; ④根据M=m/n,气体质量增加,气体物质的量不变,因此当M不变,说明反应达到平衡,故④正确;⑤题目中没有说明气体的颜色,因此颜色不变,不能说明反应达到平衡,故⑤错误;⑥没有指明反应进行方向,故⑥错误,故答案为:②④;

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案【题目】25 ℃,两种酸的电离平衡常数如下表,下列叙述正确的是( )
Ka1 | Ka2 | |
H2A | 1.3×10-2 | 6.3×10-6 |
H2B | 4.2×10-7 | 5.6×10-11 |
A. H2A的电离方程式:H2A 2H++A2-
B. 常温下,在水中Na2B的水解平衡常数为:![]()
C. 相同pH的Na2A、Na2B溶液中物质的量浓度:c(Na2A)>c(Na2B)
D. 向Na2B溶液中加入少量H2A溶液,可发生反应:B2-+H2AA2-+H2B

