题目内容
【题目】如图所示的装置,X、Y都是惰性电极.将电路接通后,向(乙)中滴人酚酞溶液,在Fe极附近显红色.试回答下列问题: 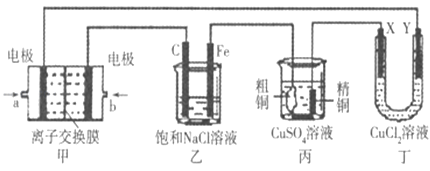
(1)(甲)装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,b处电极上发生的电极反应式是;
(2)如果(丙)装置中精铜电极的质量增加了 6.4g,则乙装置中,铁电极上产生的气体在标准状况下为L,
(3)(丁)装置中Y电极上发生的电极反应式是 .
【答案】
(1)O2+2H2O+4e﹣=4OH﹣
(2)2.24
(3)Cu2++2e﹣=Cu
【解析】解:(1)电解饱和食盐水时,酚酞变红的极是阴极,阴极和电源负极相连,则在Fe极附近显红色,所以Fe是阴极,a是负极、b是正极,C是阳极,铁是阴极,b极氧气得电子发生还原反应,电极方程式为:O2+2H2O+4e﹣=4OH﹣ , 所以答案是:O2+2H2O+4e﹣=4OH﹣;(2)乙装置中精铜电极的质量增加了6.4g,根据电极反应:Cu2++2e﹣=Cu,即生成6.4g即0.1mol铜,转移电子是0.2mol,铁电极是阴极,该极上产生氢气,2H++2e﹣=H2↑,当转移0.2mol电子时,该极上产生的气体为0.1mol,在标准状况下体积为2.24L,所以答案是:2.24;(3)(丁)装置中Y为阴极,得电子发生还原反应,电极上发生的电极反应式是Cu2++2e﹣=Cu,所以答案是:Cu2++2e﹣=Cu

练习册系列答案
相关题目


